gomoly domain (→fehérjegomoly)
Találatok címszavakban (8 szócikk):
átirat-ellenőrző gomoly* proofreading exonuclease domain az átirat ellenőrzését végző gomoly.
beágyazott gomoly másik gomolyban lévő gomoly. (→fehérjegomoly)
bromogomoly bromodomain ~110 aminosav-maradékból álló, a hisztonmag acetilezett lizinjét felismerő gomoly. Hurkok által összekötött négy α-csavarból tevődik össze. A bromogomoly az acetilezett lizinhez kapcsolódik, mint például olyanokhoz, amilyenek a hisztonmagok N-végein vannak a laza kromatinban; és továbbítja az acetilezett lizinbe foglalt jelzést, rendre fehérjék megkötésével. Pl. a hisztonmag N-végi acetilezett lizinjéhez a kromatin-ATPázok kötődnek. Ezek az enzimek elcsúsztatják a magtestecseket, miközben a DNS egy része szabaddá válik, lehetővé téve átírásfehérjék kapcsolódását.
DNS-kötő gomoly DNA binding domain a DNS-hez kötődő gomoly. (→fehérjegomoly)
fehérjegomoly* domain (domén) a fehérjében elkülönülő, 40–250 (általában 41–100)
aminosav nagyságú, önállóan (a fehérjék többi részétől függetlenül)
feltekeredő, állandósult, tömör, jellegzetes térszerkezetű, a másodlagos és a
harmadlagos szerkezeti szint közötti egység. Szokásosan β-kanyarokkal
összekötött α-csavarulat, β-lemez vagy ezek együttesének valamilyen
változatából áll. Általában a fehérjék feladatának, kapcsolódásainak a
megvalósítója, de van olyan is, amelynek elkülönült saját működése van – ez
teszi lehetővé, hogy a fehérjék többféle feladatot is ellássanak, többféle
fehérjével is kapcsolatba léphessenek, és összehangolt hálózatot hozzanak
létre. Egyes gomolyokban előfordul más molekula is, például. fémion
(hemoglobin). Általában egy képező kódol egy gomolyt, de előfordul, hogy a
közteskivágódás következtében összevágódott több képező hozza létre.
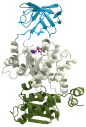 A legkisebb fehérjékben egy gomoly van, a nagyokban
akár száz is lehet. A magasabb rendű szervezetekben a fehérjék rendszerint több
gomolyt tartalmaznak jól elkülönülve; szokásosan más-más feladattal, például az
egyikkel kapcsolódik, a másik a feladatát hajtja végre. (Az ábrán a
háromgomolyos piruvát-kináz látható; forrás: Wikipédia.) Számos gomoly többféle
fehérjében is megtalálható; ezek működése különböző lehet. Vannak több egyforma
gomolyt tartalmazó fehérjék is.
A legkisebb fehérjékben egy gomoly van, a nagyokban
akár száz is lehet. A magasabb rendű szervezetekben a fehérjék rendszerint több
gomolyt tartalmaznak jól elkülönülve; szokásosan más-más feladattal, például az
egyikkel kapcsolódik, a másik a feladatát hajtja végre. (Az ábrán a
háromgomolyos piruvát-kináz látható; forrás: Wikipédia.) Számos gomoly többféle
fehérjében is megtalálható; ezek működése különböző lehet. Vannak több egyforma
gomolyt tartalmazó fehérjék is.
A gomolyok szerkezetét a másodlagos szerkezeti jelekkel és a mintázatokkal írjuk le – sokszor hozzátesszük a tekervényeket is. Bármily jellegzetesek is valamely egység mintázatai, azokból nem következtethetünk a működésére, mert előfordulhat más egységekben és a polipeptid nem tevékeny területein is.
Nemzetközi nevükben gyakorta szerepel a homology (hasonlóság) szó, utalva arra, hogy a gomoly szerkezete hasonló az abban a fehérjében lévőéhez, amelyben felfedezték. Például: PH-gomoly (pleckstrin homology domain), amelyet a pleksztrin fehérjében ismertek fel. Egyébként a nevüket általában betűszóval jelöljük. A gomolyokat síkban henger vagy doboz alakúnak ábrázolják – sokszor nevezik is őket az angol irodalomban boxoknak. Sokféle gomoly ismert. Jellegzetesebb csoportjaik:
▪ DNS-kötő gomolyok* (DNA binding domains) a DNS egyes szakaszait fajlagosan azonosítva kötődnek a DNS-sel. Szokásosan az átírásfehérjékben és a DNS-hibajavító fehérjékben találhatók. (→DNS-kötő gomolyok)
▪ Fehérjekapcsolati gomolyok* (protein interaction domains), protein–protein interaction domains, modular protein domains, protein modules a fehérjék közötti kapcsolatokat hozzák létre. Sokféle fehérjében megtalálhatók; egyazon fehérjében gyakran több is van. A fehérjekapcsolati gomolyok 40–200 aminosavat tartalmaznak, és rövid (3–6 aminosavból álló), vonalas mintázatokat (aminosavsorokat) ismernek fel (sormintázat*), ezekkel kapcsolódnak. A gomoly néhány aminosava létesít közvetlen kapcsolatot a társuló fehérjén felismert aminosavakkal, gyenge kötésekkel. Az SH2 gomoly például ~100 aminosavból áll, és foszfotirozint tartalmazó mintázatot ismer fel. Ugyancsak foszfotirozint azonosít a PTB (phosphotyrosine binding), de más mintázatban állót, mint az SH2. Az SH3 viszont többprolénes, 8–10 aminosavból álló ismétlődéseket vesz észre. Az azonosító mintázat nemcsak a kapcsolódást, hanem a ráhatást is irányíthatja, például, hogy melyik aminosav foszforileződjék. Bizonyos gomolyok a pozitív és negatív töltések elrendeződése (mintázata) szerint kapcsolódnak, és fejtik ki hatásukat – ilyen a PB1 (Phox and Bem 1) gomoly. Mintegy 85 féle fehérjekapcsolati gomolyt ismerünk. (→fehérjekapcsolódás)
▪ Kettősödési gomolyok* (dimerization domains) Bizonyos fehérjék csak kettőst képezve hatékonyak; kettősödhetnek önmagukkal (azonos kettős, homologic dimer) vagy más fehérjével (felemás kettős, heterologic dimer).
TRFH (TERF Homology Domain) a TERF1 (telomere repeat binding factor 1) vagy a TERF2 (telomere repeat binding factor 2) önmagával való párosodást hozza létre. Sajátos négyes szerkezet keletkezik. Állványként is szolgál más fehérjék társulásához, például RAP1. (→RAP1, TERF1, TERF2)
▪ Négyesítő gomolyok* (tetramerization domains) négy fehérjét összekapcsoló gomoly. Egyes fehérjék, például a p53, csak négyest alkotva hatékonyak; négy p53 fűződik egybe bennük (homotetramer).
▪ Nyolcszálas αβ-gomoly* (α/β barrel domain) nyolc párhuzamos β-lemezből és az azokat körülvevő 7–8 α-csavarulatból áll; a belső β-lemez mindegyike kapcsolódik egy α-csavarulattal, úgyhogy a szerkezet (α/β)8 szerkezetként írható le. Hordóra emlékeztető formájából származik a nemzetközi neve, ámbár nem teljesen olyan. Gyakran találunk bennük további α-, β- és más mintázatokat, sőt másik gomolyokkal is összefonódhatnak. Az ilyen enzimek családot képeznek, egyetlen „őstől” származnak, és igencsak szétágazó tevékenységűek. Jellegzetes képviselőjük a tirozinfoszfát-izomeráz, TIM1. (→TIM1)
▪ Proléngazdag gomolyok* (proline rich domains) sok prolént tartalmazó gomolyok. A fehérje sajátos térszerkezetét hozzák létre, ami elősegíti a fehérje kötődését más molekulával.
▪ Rendezetlen szerkezetű gomolyok* (intrinsically disordered domains, IDDs) jellegzetes mintázat és sajátosság nélküli, alig tekeredett gomolyok; térszerkezetüket könnyen változtatják. Mivel szerkezetük kevéssé kötött, rugalmasan, nagyobb alkalmazkodással képesek részt venni nagyon különböző biológiai folyamatokban (felismerésben, szabályozásban, jelközvetítésben). A magasabb rendű szervezetekben gyakoribbak, ami arra utal, hogy a fehérjék törzsfejlődésének magasabb fokozatai. Jelentősek a kutatás szempontjából is: a szerkezetkutatás fordított megközelítésének módja – a mintázathiány felől közelíthetők meg a szerkezeti összefüggések.
▪ RING (really interesting new gene) gomoly (RING finger domain/protein) C3HC4 aminosav-mintázatot és két cinkiont tartalmaz. 40–60 aminosavból áll; központi α-csavarodással és szegélyező két hurokkal, amelyeket a cinkion rögzít. Az ubikvitjelölésben van meghatározó szerepe, állványfehérjeként vesz részt: nem köti az ubikvitint elektronkötéssel. A RING gomolyt tartalmazó fehérjéket RING fehérjéknek nevezzük. (→ubikvitinezés)
▪ RNS-kötő gomolyok* (RNA binding domains) az RNS egyes részeit, rendre a végeket, fajlagosan azonosítva kötődnek az RNS-sel. (→RNS-kötő gomolyok)
▪ Sarkallógomolyok* (catalytic domains) az enzimek hatóegységei. Általában törzsökös szerkezetűek, és jellegzetesek az enzimcsoportokra. Például a kinázok mindegyikében ~250 aminosavból álló, sajátos térszerkezetű foszforilező gomoly van (kinázgomoly).
▪ Kölcsöntevősítő gomolyok* (transactivation domains, TAD) állványfehérje, több fehérjét köt, megteremtve kölcsönhatást közöttük, hogy kölcsönösen tevősödjenek.
▪ Beágyazottt gomly* olyan gomolyak, amelyek másik gomolyban vannak. Ilyen például az E2F1 fehérjecsalád daganatgátló-társulási gomoly, amely a kölcsönhatást serkentő gomolyba van beépítve.
kromogomoly* chromodomain ( chromatin organization modifier) a kromatinnal társult, módosulásait végző fehérjék sajátos gomolya. ~50 aminosav-maradékból álló, a hisztonmag metilezett lizinjét felismerő törzsökös gomoly. Három β-lemezből és egy α-csavarulatból tevődik össze. A kromogomolyt tartalmazó fehérjék elősegítik a kromatin tömörödését, gátolják a génátírást. Ezeket a fehérjéket három csoportba soroljuk:
▪ Az elsőbe azok tartoznak, amelyekben az N-végi kromogomoly után árnyék kromogomoly van. Ilyen például a HP1 fehérje. Az árnyék kromogomoly* csak kromogomollyal együtt fordul elő (innen az „árnyék” jelző), a magtestecseket közelítik egymáshoz. Az ilyen fehérjék tehát tömörítik a kromatint.
▪ A másodikba tartozóknak csak egyetlen kromogomolya van (például polycomb).
▪ A harmadikba tartozókban kettőzött a kromogomoly (például DNS-kötő helikázok, CHD1–CHD4).
RRM gomoly ( RNA Recognition Motif) (→RNS-kötő gomolyok)
WD40 gomoly WD40 repeat domain, WDR ismétletekből és ~20 aminosav-maradéknyi változó részből áll. Az ismétletek sajátos ellentétes négyszálas β-lemezt (β-lapát) formálnak. Ezek a lapátok összekapaszkodva β-hajócsavart alkotnak, a leggyakoribb a hétlapátos β-hajócsavar. Ez a merev hajócsavarszerű szerkezet állékony felszínt biztosít fehérjék kapcsolódásához, létrehozva kölcsönhatásokat közöttük.
Találatok alcímszavakban (1 szócikk):
DNS-kötő gomolyok DNA binding domains, DBDs a DNS 4–12 bázispárnyi szakaszával fajlagosan kötődő gomolyok. A DNS-kötő fehérjéket ezek alapján csoportosítjuk. Többféle mintázatúak, pl. előfordul bennük:
▪ cinkujj* mintázat (zinc finger motif) 25 aminosavnyi ujjszerű hurokmintázat, amelyben négy állandó aminosav (két cisztein, két hisztidin) két cinkiont köt; ezek ismétlődnek egymás után.
▪ α-csavarodás–hurok–α-csavarodás* mintázat (helix-loop-helix motif) hurokelemmel lazán összekötött, egymást fedő α-csavarodások;ez a leggyengébb kapcsolásmintázat.
▪ leucinos zármintázat* (leucine zipper motif) kétfordulatú csavarmenetszerű aminosavsor, amelyben minden hetedik aminosav leucin; ez ismétlődik mindkét fordulatban.
▪ α-csavarodás–fordulás–α-csavarodás* mintázat (helix-turn-helix motif) rövid kapcsolóval összekötött, DNS-fajlagosan összekapaszkodott két α-csavarodás. Stb.
bZIP gomoly (basic leucine zipper domain) víztaszító leucinben és lizin–argininben gazdag felismerő részeket tartalmaz – az előző a kettőződést, az utóbbi a DNS-hez kapcsolódást hozza létre.
cinkujj gomoly* zinc-finger domain több, ujjszerű alakulatot (cinkujj mintázat) tartalmaz; képes az RNS-sel is társulni.
MYB (vírusfehérje [avian myelo blastomatosis virus] nevéből származik) a kromoszómák végrészének kétszálú DNS-éhez fajlagosan kapcsolódó gomoly; a GGTTAG/CCAATC mintázatot ismeri fel.
Részleges egyezések (14 szócikk):
α/β barrel domain nyolcszálas αβ-gomoly nyolc párhuzamos β-lemezből és az azokat körülvevő 7–8 α-csavarulatból tevődik össze. (→fehérjegomoly)
catalytic domains sarkallógomolyok az enzimek hatóegységei. (→fehérjegomoly)
dimerization domain kettősödési gomolyok bizonyos fehérjék azonos fehérjék való összekötődését elősegítő gomoly. (→fehérjegomoly)
fehérjeszerkezet A fehérjék szerkezetében négyféle szerkezeti szintet (elsődleges, másodlagos, harmadlagos és negyedleges) különböztetünk meg. Ez kiegészül a második és a harmadik szint közötti két másodfeletti elemmel (gomoly, mintázat). Mindegyik szintet az aminosavak sora határozza meg.
elsődleges szerkezet a peptidkötéssel kapcsolt aminosavmaradék-sor. Voltaképpen a polipeptid. Az átlagos fehérje 300–400 aminosav-maradékból áll, tömege: ~40 kDa. Van 50 és 2000 aminosav-maradékból összetevődő is, a fehérjék aminosav-maradék tartománya tehát: 50–2000 aminosav-maradék.
másodlagos szerkezet az aminosavsor elfordulásaiból keletkező alakzat, amelyet az egymáshoz közel kerülő atomok közt kialakuló hidrogénkötések rögzítenek. Hidrogénhíd keletkezik a peptidkötés O- és N-atomja között; ez könnyen kialakul az oxigén és a nitrogén részleges ellentétes töltése miatt. A másodlagos kapcsolódások tehát a polipeptid gerincében jönnek létre, az aminosavak oldalláncai nem vesznek részt benne.
Elfordulás az aminosavak oldalláncainak különbözősége (kiegyensúlyozatlan állapot) révén következik be, és a peptidkötés elektroneltolódása miatt csak az α-szénatom kétoldali kötésében lehetséges, ezek szigma-kötések. Az N–Cα kötés elfordulásának szöge a φ-szög, Cα–C kötésé a ψ-szög (→peptidkötés). A φ–ψ szögpárok által létrehozott térhelyzetben az N–Cα–C–N atomsorból szabályosan ismétlődő szerkezetek jönnek létre; ezek a másodlagos szerkezetek. Kialakulásuk a szögpárok értékeitől függ; azokat az értékeket, amelyeknél kialakulhatnak, a Ramachandra-leképezés mutatja. A szögpár nagysága azonban a peptidkötések atomjai és az oldalláncok helyzete miatt behatárolt; a másodlagos szerkezetek létrejöttéhez szükséges értékek a polipeptidnek csak egyes részein (elfordulási sziget) jönnek létre, függően az aminosavsortól: attól, hogy milyen aminosavak kapcsolódnak egymással.
A legjellegzetesebb másodlagos szerkezeti elemek az α-csavar, a β-lemez és a β-fordulat.
 ■ α-csavarodás (α-helix) a
peptidlánc csavarvonalszerű elfordulásával keletkezik. Egy menetben 3,6
aminosav-maradék van. A peptidkötések közötti hidrogénhidak szabályos
távolságonként ismétlődnek – minden negyedik peptidkötést kapcsolják a
karbonil- és az NH-csoport között (CO…NH) –, és a molekula hossztengelyével
csaknem párhuzamosan helyezkednek el; ezért keletkezik a csavarvonal szerkezet.
Az aminosavak oldalláncai a hossztengelyre merőlegesen, a csavarmenet külső
felszínén találhatók, a víztaszító gerinc pedig a belsejében. Az órajárás
irányában haladó elfordulások hozzák létre az α-csavarodást, amely állandósult
szerkezet. Ez az aminosavak L-téralakzatából következik. A csavarodás
végbemehet ellenkező irányban is, de az ilyen szerkezetek ingatagok: az
oldalláncok térben nehezen férnek el, ezért nem is maradnak meg.
■ α-csavarodás (α-helix) a
peptidlánc csavarvonalszerű elfordulásával keletkezik. Egy menetben 3,6
aminosav-maradék van. A peptidkötések közötti hidrogénhidak szabályos
távolságonként ismétlődnek – minden negyedik peptidkötést kapcsolják a
karbonil- és az NH-csoport között (CO…NH) –, és a molekula hossztengelyével
csaknem párhuzamosan helyezkednek el; ezért keletkezik a csavarvonal szerkezet.
Az aminosavak oldalláncai a hossztengelyre merőlegesen, a csavarmenet külső
felszínén találhatók, a víztaszító gerinc pedig a belsejében. Az órajárás
irányában haladó elfordulások hozzák létre az α-csavarodást, amely állandósult
szerkezet. Ez az aminosavak L-téralakzatából következik. A csavarodás
végbemehet ellenkező irányban is, de az ilyen szerkezetek ingatagok: az
oldalláncok térben nehezen férnek el, ezért nem is maradnak meg.
Az α-csavarodás a polipeptidnek csak hosszabb-rövidebb szakaszain alakul ki: egyes helyeken megszakad, mert a hidrogénhíd nem jön létre. Ennek több oka lehet:
• A prolin gyűrűs szerkezetében a nitrogénatomnál nem áll rendelkezésre hidrogénatom, és a fordulása is korlátozott; ezért nincs gyűrűs aminosav az α-csavarvonal szerkezetben.
• Egymást taszító aminosavak között, például két arginin között (negatív töltésű az oldallánc).
• Túl nagy az oldallánc; a társulás térben nem lehetséges, ilyen a fenilalanin.
Az α-csavarodás elhelyezkedhet a fehérje bármely részén; átlagosan 12 aminosav-maradék hosszúságú, az N-vége részpozitív, a C-vég résznegatív, vagyis kétsarkú (dipole) szerkezet.
■ β-lemez (β sheet). Megnyúltan csavarodó peptidláncból alakul ki a lánc visszakanyarodásaival (β-fordulás). A peptidlánc ebben is csavarvonalszerű, de egy kanyarulatban csak két aminosav van, ezért lapos. A visszakanyarodás következtében néhány aminosavnyi peptidszakasz (β-redő, β strand) párhuzamosan helyezkedik el – egy irányban vagy ellentétesen (az egyiknek az N-vége és a másiknak a C-vége van egymás mellett) –, közöttük pedig hidrogénkötések képződnek, amelyek itt is a peptidkötések karbonil- és NH-csoportja között (CO…NH) jönnek létre.
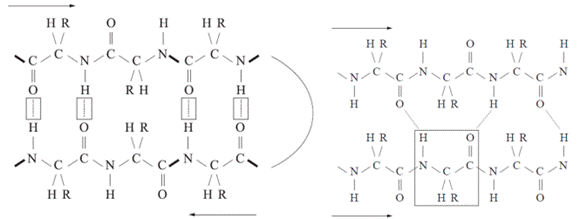 Az első ábrán a két β-szál egymással ellentétes irányú
(antiparallel). A közöttük keletkező hidrogénhíd a szemben lévő peptidkötések
mindegyikében kialakul, éspedig a hossztengelyére merőlegesen, mivel a CO- és
NH-csoportok szemben vannak egymással. Az oldalláncok kívül helyezkednek el. A
második ábrán a megnyúlt polipeptidlánc (β-szál) visszakanyarodik (β-fordulás,
β-turn), és az előző szakaszával azonos irányú (parallel). A hidrogénhidak itt
is keresztezik a hossztengelyt, de nem merőlegesek. Egy aminosav két szemközti
aminosavval kapcsolódik.
Az első ábrán a két β-szál egymással ellentétes irányú
(antiparallel). A közöttük keletkező hidrogénhíd a szemben lévő peptidkötések
mindegyikében kialakul, éspedig a hossztengelyére merőlegesen, mivel a CO- és
NH-csoportok szemben vannak egymással. Az oldalláncok kívül helyezkednek el. A
második ábrán a megnyúlt polipeptidlánc (β-szál) visszakanyarodik (β-fordulás,
β-turn), és az előző szakaszával azonos irányú (parallel). A hidrogénhidak itt
is keresztezik a hossztengelyt, de nem merőlegesek. Egy aminosav két szemközti
aminosavval kapcsolódik.
A többszörösen egymáshoz kötődött β-szálak alakítják ki a β-lemezt, amelyből az oldalláncok kilógnak: felettük és alattuk helyezkednek el. Az egymáshoz kapcsolódó β-szálak származhatnak egyetlen polipeptidből, de kapcsolódhat hozzájuk másik polipeptid β-szála is (ábra). A β-szálak különbözősége miatt a β-lemez nem sík, hanem redőzött (pleated β sheet).
Az aminosavak oldalláncai a lemez síkja felett vagy alatt nyúlnak ki úgy, hogy a sorban egymást követő aminosavak oldalláncai ellentétes kinyúlásúak, ezért redőszerű, hajtogatott. A párhuzamos β-redőket hosszabb-rövidebb aminosavszakaszok kapcsolják össze; nemegyszer úgy, hogy a β-lemez síkja felett/alatt α-csavar szerkezeteket alakítanak ki. Az ellentétesen futó β-redőket néhány helyen aminosavas visszafordulások kötik össze; ilyen pl a hajtűfordulás* (hairpin turn), amely két ellentétes irányú β-szál között keletkezik; összesen két aminosav-maradékból áll. A β-lemez lapszerű, gyakorta hajtékolt, nagyritkán hengeres formájú, és szokásosan a fehérje belsejében van: a víztaszító peptidgerinc ugyanis szabadon van.
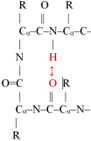 ■ β-fordulás* (β-turn, β-reverse turn, β-bend). A polipeptid egyirányú, ezért gömbalakot csak úgy hozhat
létre, hogy visszafordul. Az ilyen visszafordulás a β-fordulás, amely nagyon
rövid szakasz, hajtűszerű. Ezek kapcsolnak össze két α-csavart vagy két
β-szálat. A β-fordulat négy aminosav-maradékból áll. A hidrogénhíd a polipeptid
visszafordulását kezdő és a harmadik aminosavát köti; ezzel rögzíti a
szerkezetet (az ábrán pirossal jelölve; R = oldallánc). I-es és II-es formáját
különböztetik meg. A β-fordulás sokszor a fehérje felszínén van, részt vesz a jelközvetítésekben
kapcsolódási vagy felismerési helyként.
■ β-fordulás* (β-turn, β-reverse turn, β-bend). A polipeptid egyirányú, ezért gömbalakot csak úgy hozhat
létre, hogy visszafordul. Az ilyen visszafordulás a β-fordulás, amely nagyon
rövid szakasz, hajtűszerű. Ezek kapcsolnak össze két α-csavart vagy két
β-szálat. A β-fordulat négy aminosav-maradékból áll. A hidrogénhíd a polipeptid
visszafordulását kezdő és a harmadik aminosavát köti; ezzel rögzíti a
szerkezetet (az ábrán pirossal jelölve; R = oldallánc). I-es és II-es formáját
különböztetik meg. A β-fordulás sokszor a fehérje felszínén van, részt vesz a jelközvetítésekben
kapcsolódási vagy felismerési helyként.
■ Rendezetlen fehérjeszakaszok. Ezek a fenti mintázatok egyikét sem tartalmazó részei a fehérjéknek, általában a fehérjék zömét alkotják. A fehérjék alkalmazkodó képességét (kapcsolódás más molekulával, térszerkezeti változás stb.) biztosítják, lehetővé téve a fehérjék tevékenységének szabályozását. Talán idevehető a kapocsrész (hinge region), amely változó hosszúságú hajlékony aminosavmaradék-sor, szokásosan két gomoly között. Lehetővé teszi, hogy a gomolyok elmozduljanak egymáshoz viszonyítva feladatuk ellátására. Nincs mindegyik fehérjében. A korábbi irodalomban találkozunk a Ω-hurok (Ω loop) elnevezéssel, amely rendszertelen, ismétlődő részek nélküli bonyolult szerkezetű fehérjealakzat. Megkülönböztetése nem megalapozott.
másodfeletti elemek a →fehérjegomolyok és a →fehérjemintázatok.
harmadlagos szerkezet tertiary protein structure a fehérje (egyetlen polipeptid) háromirányú (3D) elrendeződése, működőképessé válása; a hatócsoportok a felszínre kerülnek, lehetővé téve, hogy kapcsolatba lépjenek más molekulákkal. A harmadlagos szerkezet az egymástól távoli aminosavak közötti kölcsönhatások, alapvetően az aminosavak oldalláncai között létrejövő kötések (leginkább hidrogénkötések, ritkábban S–S- és ionos kötések), valamint a víztaszító hatás következménye. A harmadlagos szerkezetet tehát a peptidkötések mellett kialakuló más elektron- és nem elektronkötések hozzák létre, tartják fenn. A harmadlagos szerkezet elsősorban a gombolyagfehérjékben alakul ki, a szálas fehérjékben (→keratin, kollagén, fibroin) kevéssé kifejezett, nem különül el élesen; térszerkezetüket valamelyik másodlagos szerkezeti elem uralja. A fehérjék a harmadlagos szerkezeti formában állandók, az energia szempontjából ez a leggazdaságosabb helyzetük (native state).
A harmadlagos térszerkezetet is alapvetően az aminosavak sorrendje határozza meg, és önmagától is kialakul. A dajkafehérjék (chaperonok) elősegítik a harmadlagos szerkezet formálódását: megakadályozzák, hogy a sejtplazmában állandóan keletkező fehérjék – a harmadlagos szerkezet lassú formálódása miatt – egymással összekapaszkodjanak fehérjehalmazokká.
Lényeges, hogy a fehérjék harmadlagos szerkezete környezeti és más hatásokra (más fehérje társulása, foszforilezés stb.) felszakadhat, tehát nem állandó. Ennek biológiai jelentősége van, hiszen a térszerkezet változása, változtatása a fehérjék ki-be kapcsolásának a leggyakoribb módja, a fehérjeműködés alapvető szabályozója.
negyedleges szerkezet quaternary protein structure két vagy több harmadlagos szerkezetű polipeptid kapcsolódásából létrejövő nagymolekula (többes fehérje). Az egyes polipeptideket alegységeknek nevezzük. A negyedleges szerkezet az alegységek egymáshoz viszonyított térhelyzetét jellemzi. A polipeptidek közötti kölcsönhatásban ugyanazok a kötések (London-erők, hidrogénkötések, ionkötések és S–S híd) vesznek részt – vagyis alapvetően gyenge kötések.
A polipeptidek száma szerint megkülönböztetünk kéttagú (dimer, kettős), háromtagú (trimer, hármas), négytagú (tetramer, négyes) stb., pártagú (oligomeric proteins) és soktagú (polymer) fehérjéket. Ezek ekként, tehát kéttagúként, háromtagúként stb. hatásosak. Kapcsolódhat azonos (homo-…mer) vagy különböző polipeptidlánc (hetero-…mer).
Az összekapcsolódott polipeptidek szétválhatnak, majd újra egyesülhetnek, függően a működésüktől. A szétválást, újra egyesülést az teszi lehetővé, hogy azokon a felületeken, ahol a kötődés létrejön, egymást kiegészítő molekulák vannak – a kiegészítő láncok egymást felismerik –, és hogy a nem kiegészítő láncok között nem képződik erős kapcsolódás. A polipeptidek között tehát egy sajátságos kölcsönhatás van, amely a fehérjék működését is meghatározza, szabályozza – ez a fehérjék önrendelkező képessége.
Negyedleges szerkezetűnek tartjuk a más molekulát (hem, szénhidrát, RNS, lipid stb.) tartalmazó fehérjét is.
intrinsically disordered domains, IDDs rendezetlen szerkezetű gomoly jellegzetes szerkezet nélküli gomoly. (→fehérjegomoly)
prolene rich domains proléngazdag gomoly a fehérjék térszerkezetének alakulásában van szerepe.
protein interaction domains, protein–protein interaction domain fehérjekapcsolati gomolyok fehérjékkel kacsolódó gomolyok, köztük kölcsönhatásokat hoznak létre.
rendezetlen szerkezetű gomolyok* intrinsically disordered domains, IDDs (→fehérjegomoly)
RING (really interesting new gene), RING finger domain/protein RING gomoly az RNS hurkaihoz kötődő gomoly. (→fehérjegomoly)
RING ( really interesting new gene) finger domain RING gomoly (→fehérjegomoly)
RNA binding domain RNS-kötő gomoly az RNS-ekhez kapcsolódó gomoly. (→fehérjegomoly)
RNS-kötő gomolyok* RNA binding domains, RBD az RNS-t célzottan azonosító, általában valamilyen, RNS-t felismerő mintázatot tartalmazó gomolyok. Ezek kötődnek célzottan az RNS-sel. Egyesek az RNS néhány bázisnyi részét, mások szerkezeti elemeket ismernek fel. A néhány bázisnyit azonosítók általában nem fajlagosak, ezért belőlük több van a fehérjében, együttesen biztosítják a fajlagosságot.
Az RNS-kötő/felismerő gomoly, illetve RNS-felismerő/kötő mintázat elnevezések használata messze nem egységes a nemzetközi irodalomban, sőt előfordul, hogy ugyanazt gomolynak és mintázatnak is nevezik; a kettőt felcserélve használják. Ezért a gomoly és a mintázat megkülönböztetése ebben az összefüggésben nem lehetséges.
Hozzávetőlegesen 50-féle RNS-kötő gomoly ismert; a leggyakrabban előfordulók:
▪ RNS-felismerő mintázat (RNA-recognition motif, RRM). (Egyéb elnevezési: ribonucleoprotein [RNP] motif, RNP-type RNA-binding domain [RBD], RNP domain) ~80 aminosav-maradékból áll; két ellentétes négyszálas β-lemez és az ezeket összekötő két α-csavarodás alkotja, β-α-β-β-α-β szerkezetű. A két középső β-szálban két törzsökös bázismintázat, az RNP1 (nyolcbázisos) és az RNP2 (hatbázisos) található. Az RNS-kötő fehérjék többségében fellelhető; egyszálú RNS-sel kapcsolódik.
▪ Kétszálú RNS-t kötő gomoly (double strand RNA binding domain, dsRBD) rövid bázismintázat, ~70 aminosav-maradékból áll. Egy ellentétes háromszálú β-lemez és egy-egy C-, ill. N-végi α-csavarodás alkotja. Sokféle eltérő tevékenységű fehérjében fordul elő, jóformán csak a kétszálú RNS-hez kötődik – az egyszálúhoz nem, és a DNS-hez sem.
▪ KH gomoly (K homology sequence domain) a hnRNPk fehérjében azonosították. Két rövid bázismintázat, mindegyik ~70 aminosav-maradékból áll és egy ellentétes háromszálú β-lemezből, valamint három α-csavarodásból tevődik össze β-α-α-β-β-α szerkezetben. Több mint százféle fehérjében fordul elő.
RNS-kötő álgomolyok pseudo-RBD olyan gomolyok, amelyek nem kötődnek az RNS-hez, de van szerepük a fehérje–RNS kapcsolódásban.
tetramerization domain négyesítő gomoly négy fehérjét összekapcsoló gomoly. (→fehérjegomoly)
transactivation domain, TAD kölcsöntevősítő gomoly kölcsönhatást teremtő állványfehérje. (→fehérjegomoly)