közteskivágás* gene splicing, pre-mRNA splicing (elő-mRNS-kivágás) a génátíródást követő módosítás, az elő-mRNS (érett) mRNS-sé alakítása. Lényege az elő-mRNS közteseinek kivágása és a képezők egyesítése különböző változatokban; vagyis többféle érett mRNS (testvérmások, isoforms) keletkezhet, amelyekről más-más szerkezetű és tevékenységű fehérjék képződnek. Ez teszi lehetővé, hogy egyetlen génről többféle fehérje képződjék; ez a fehérjék sokféleségének egyik leggyakoribb kialakulási módja. Például az SLO génről 500 testvérmás keletkezhet. Az emberi DNS-ben ~20 000 fehérjét kódoló gén van, de >100 000-féle fehérje képződik. A közteskivágást az RNS-szike végzi, a sejtmagban megy végbe, és részese a génműködés szabályozásának. Hozzávetőlegesen az elő-mRNS-ek 90%-ában lejátszódik. Az esetek többségében a génátíródással egyidejűleg történik, a többiben utána, de még a sejtmagban. A kivágás a sejtműködés, az egész élet alapfolyamata. Az RNS-szike és kapcsolódó fehérjék hibái kétszáznál is több betegséget okoznak, rákképződést is. A daganatgátló és daganatserkentő gének részt vesznek az átíródást követő szabályozásokban, elősegítve a rák kialakulását, pl. a MYC átírásfehérje, amely gyakran hibás a ráksejtekben, közreműködik az elő-mRNS kivágásában.
A testvérmások többféleképpen jöhetnek létre:
- az összes köztes kivágásával, és a képezők hiánytalan egyesülésével,
- nem az összes köztes kivágásával,
- egy-egy képező vagy képezők részeinek kivágásával,
- ezek különböző változtatásával. (→elő-mRNS–mRNS átalakítás)
A közteskivágásnak két formája ismert: a teljes és a kiválasztó közteskivágás.
▪ A teljes közteskivágásban* (constitutive splicing) az adott génben található minden köztes kivágódik és valamennyi képező benn marad az érett mRNS-ben.
▪ Kiválasztó közteskivágáskor* (alternative splicing) egy adott köztes nem mindig vágódik ki; illetve egy adott képező nincs mindig jelen az érett mRNS-ben, ezért testvérmások keletkeznek.
Megkülönbeztetik még az eltérő kivágást, amely a szokványostól eltérő szerkezetű köztes kivágása, pl. az U12-es féle köztes U12-type intron – amelyben nincs 5’-vágáspont és A-elágazás – másként vágódik ki: sajátos, piciny RNS-szike* (minor spliceosome) távolítja el a köztest.
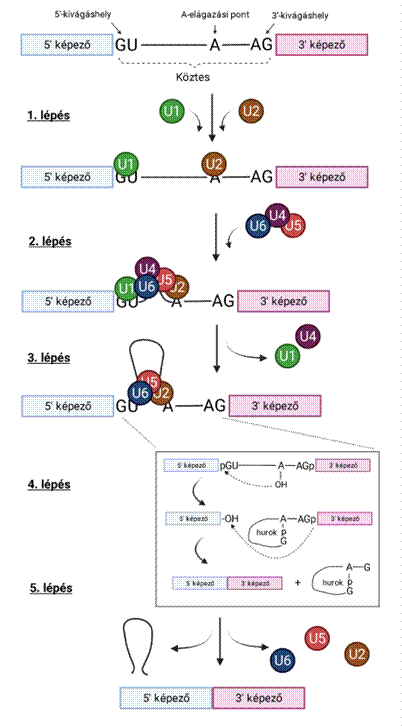 Első és második lépés: Először az U2 (U2snRNP) kapcsolódik az A-elágazáshoz. Az RNS-szike
ennek alapján azonosítja a kivágandó részt, ezzel indul a folyamat. Az U2
törzsökös GTAGTA hatosa bázispárosodással társul az A-elágazással, amelynek
törzsökös adenozinja ennek következtében előemelkedik. Az U2 társulásának
hatására az U1 (U1snRNP) az 5’-kivágáspont GU bázisaival kötődik, majd (második
lépés) az U4-, U5- és U6 kapcsolódik az U2- és U1-hez, áthidalva a köztük lévő
távolságot. Az UsnRNP kapcsolódására az 5’-kivágáshely és az A-elágazás, főleg
annak törzsökös adenozinja, közel kerül egymáshoz.
Első és második lépés: Először az U2 (U2snRNP) kapcsolódik az A-elágazáshoz. Az RNS-szike
ennek alapján azonosítja a kivágandó részt, ezzel indul a folyamat. Az U2
törzsökös GTAGTA hatosa bázispárosodással társul az A-elágazással, amelynek
törzsökös adenozinja ennek következtében előemelkedik. Az U2 társulásának
hatására az U1 (U1snRNP) az 5’-kivágáspont GU bázisaival kötődik, majd (második
lépés) az U4-, U5- és U6 kapcsolódik az U2- és U1-hez, áthidalva a köztük lévő
távolságot. Az UsnRNP kapcsolódására az 5’-kivágáshely és az A-elágazás, főleg
annak törzsökös adenozinja, közel kerül egymáshoz.