térhelyzeti azonmások* conformational isomers, conformers, rotational isomers ugyanazon molekula egyszeres elektronkötése mentén való elfordulásokból létrejöhető térszerkezeti változatok. Egymásba könnyen átfordulnak. A térhelyzeti azonmások tehát az elektronkötések felbomlása nélkül alakulhatnak át egymásba.
Ha az azonmásságot kialakító két molekula egyirányú, szün,
ha ellentétes, anti helyzetről beszélünk. Ezt nevezzük szün–anti
azonmásságnak. Pl.: a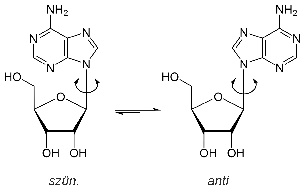 z adenozin szün helyzetében a cukor ötödik
szénatomjához kapcsolt OH-csoport és a gyűrűs molekula aminocsoportja (a két
molekularészlet nem kapcsolódik egymással) egyirányú, az anti
helyzetében ellentétes.
z adenozin szün helyzetében a cukor ötödik
szénatomjához kapcsolt OH-csoport és a gyűrűs molekula aminocsoportja (a két
molekularészlet nem kapcsolódik egymással) egyirányú, az anti
helyzetében ellentétes.
Az elforgatással az egyik (A) térhelzeti azonmás átmenetformán (transition state) keresztül átalakul a másik (B) térazonmássá. Az A és a B térazonmás helyi energiája a legkisebb, az átmenetállapoté a legnagyobb. A forgatás az energiakülönbséget (energiagát*) küzdi le. Ha az energiagát kicsi, a két térazonmás könnyen és gyorsan átalakul, szokásosan mindkettő jelen van, váltakozó egyensúlyi állapotban. Ha az energiagát nagy, a forgatás korlátozott, az átmenetalakzat tartósan jelen lehet külön molekulaként; ezt a molekulát nevezzük átmeneti térazonmásnak* (rotational isomer, rotamer). A hosszan megmaradó és ezért elkülöníthető átmeneti térazonmást veszteglő térazonmásnak* (atropisomer) mondjuk.