DNS (dezoxiribonukleinsav) deoxyribonucleic acid, DNA az élőlények létezését lehetővé tevő genetikai üzenetet hordozó molekula. Két szálból (DNS-szál) áll, amelyek csavarmenetszerűen egymás köré tekerednek (kettős csavarulat). Mindegyik szálnak dezoxiribózból és foszfátból álló gerince van. Minden dezoxiribózhoz egy-egy bázis kötődik a citozin, adenin, timin vagy guanin közül. A bázisok sorrendje a genetikai kód, ez határozza meg, hogy milyen RNS (fehérje) keletkezik. A két DNS-szál bázisaival kötődik egymáshoz. Az emberi DNS hozzávetőlegesen 3 billió bázispárt tartalmaz, és 99,7%-a minden emberben egyforma. Csupán 0,3% nagyságú az a DNS-rész, amely megkülönbözteti egyik embert a másiktól a genetika szintjén. Ezek a DNS-szakaszok az ismétletek, ezek különböznek egyénenként, anélkül, hagy hatással lennének a genetikai egészségre.
genom (DNS) genome a sejt teljes DNS-ében rejtett genetikai tartalom összessége. (Vírusokban a DNS-ben vagy az RNS-ben rejtőző genetikai tartalom egésze.) Az emberi genom a sejtmagban lévő 23 kromoszómapárból és az energiatermecsben lévő DNS-ekből tevődik össze (3 milliárd nukleotid). Tartalmazza az egyén létezéséhez és tevékenységéhez szükséges összes ismeretet. A napi szóhasználatban DNS mondható a genom helyett. (→energiatermecs-DNS, vírusgenom)
Találatok címszavakban (49 szócikk):
DNS-átalakulás a DNS szerkezetének élettani változása, pl. DNS-kettőződésben.
DNS-átrendeződés DNA recombination (homologous recombination) a kettős DNS-szál egy darabjának az eredetihez hasonló, majdnem azonos másik DNS-szállal való helyettesítése. Pontosan nem egyezik a kettő, de az eltérés nem befolyásolja a DNS működését.
DNS-elemek a DNS működési egységei. Olyan DNS-szakaszok (bázissorok), amelyek valamilyen sajátos tulajdonságúak, sajátos tevékenységet végeznek. Ezek nem határolódnak el valamiféle elválasztóval: a bázissor folyamatos, a bázisok összeállása különíti el őket. Az egyes elemeknek lehetnek saját elemeik is; ezeket nem tartjuk önálló feladatú DNS-működési egységnek. Ötféle elemet különböztetünk meg. Ezek:
▪ Fehérjekódoló gének (protein coding genes), amelyek a DNS törzselemét képezik, mégis csupán a DNS 1–2%-át foglalják el. A fehérjét kódoló géneknek lényegében négy eleme van (génelemek), a képező, a köztes, az indító és a szabályozó rész. Noha a képezők (exonic sequences) és a köztesek (intronic sequences) tevékenysége lényegileg eltér, ezeket mégsem tekintjük különálló DNS-egységnek, mert egyféle tevékenység, a fehérjeképzés részei. (→génszerkezet, indító, képező, köztes)
▪ Nem kódoló RNS-t képező gének (non-coding (nc) RNA genes); azok a gének, amelyek nem az mRNS-t kódolják.
▪ Szabályozó bázissorok (regulatory elements, cis-acting regulatory elements, CREs) az átíródást irányításában résztvevő elemek; DNS-beli szabályozók. Ezek a fokozók, a csillapítók, insulators… Számukat több mint 1 millióra becsülik. (→csillapítók, fokozók ).
▪ Ismétletek (repeats), a DNS 70 %-át kitevő, egymást követően vagy szétszórva a DNS különböző részein ismétlődő bázissorok. Helyük állandó, számuk jellegzetes az egyedre (→ismétletek)
▪ Ugrálatok (transposons) a helyüket változató bázissorok. A DNS ~50%-át teszik ki. Vannak köztük egymás után ismétlődők is, ezért az ismétleteket és az ugrálatokat a nemzetközi irodalom közös nevezettel, repetitive DNA illetik. Az ismétletek és az ugrálatok alapvetően a szabályozókkal vannak kapcsolatban. (→ugrálat)
Nem önálló egységek a DNS-válaszelemek, amelyekből nagyon sokféle ismert. (→DNS-válaszelemek)
DNS-enzimek a DNS-sel (dezoxiribonukleinsavval) kapcsolatos enzimek.
▪ DNS-t bontó enzimek (→DNáz, DNS-glikoziláz, DNS-helikáz)
▪ DNS-t egyesítő enzim (→DNS-ligáz)
▪ DNS-t hasító, újraegyesítő enzimek (→DNS-topoizomeráz)
▪ DNS-t képző enzimek (→DNS-polimeráz, DNS-telomeráz)
▪ DNS-t metilező és demetilező enzimek (→DNS-metil-transzferáz)
DNS-fehérjeköpeny nucleocapsid (nukleokapszid)
(→víruszerkezet)
DNS-féleség* a különféle alapszerkezetű DNS-ek valamelyike. Pl. aDNS, bDNS stb. (→DNS)
DNS-giráz DNA gyrase a 2-es formájú topoizomeráz (TOP2), a DNS-lánc széttekeredését (alultekeredés) végzi az ATP-ből származó energia felhasználásával. A DNS-kettőződés, -átíródás, DNS-hibák javításában stb. van szerepe: töri a kettős DNS-t. Többek közt DNS-t törő és ATP-kötő gomolya van. (→DNS-topoizomerázok)
DNS-hiba a DNS bázisainak és vagy gerincének olyan eltérése, amely megváltoztatja a DNS működését; átíródást vagy kettőződést. Többféle ismert:
DNS-károsodás a DNS gerincének kóros (nem élettani) átalakulása változásoktól a DNS kettőstöréséig sokféle lehet.
DNS-hiány DNA gap egy vagy több bázis hiánya. A DNS-szál megtartott, de alakja változhat.
DNS-hézag DNA nick esetén a bázisok mind megvannak, csak a DNS-gerinc (backbone) nem egyesített.
DNS-hibaválasz fehérje* DNA damage protein a DNS-hibát felismerő, a javítást elindító fehérje.
DNS-ismétlet →ismétlet
DNS-károsodási válasz DNA damage response (DDR) a DNS károsodásának hatására elkezdődő molekulatörténések. Magában foglalja a DNS károsodását felismerő és javító folyamatokat.
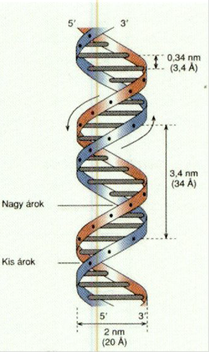 DNS kettős csavarodás* double helix A két csavarmenetű DNS-szál egymás
köré tekeredik ellentétes irányban (az egyik 5’→3’ a másik 3’→5’ helyzetű). Ezt
a szerkezetet nevezzük kettős csavarodásnak*; ez a kettős DNS-szál alakja. A
kettős szál átmérője 2 nm. A bázisok síkja a tengelyre merőleges, de a bázisok
egymáshoz viszonyítva 36o-kal elfordulnak, a köztük lévő távolság
0,34 nm. A csavarlat egy-egy 360º-os fordulata között tehát 10 nukleotid
található, a csavarulat távolsága pedig 3,4 nm. Az ettől eltérő tekeredés a
túltekeredés (supercoiling), amely lehet negatív és pozitív.
(→DNS-túltekeredés).
DNS kettős csavarodás* double helix A két csavarmenetű DNS-szál egymás
köré tekeredik ellentétes irányban (az egyik 5’→3’ a másik 3’→5’ helyzetű). Ezt
a szerkezetet nevezzük kettős csavarodásnak*; ez a kettős DNS-szál alakja. A
kettős szál átmérője 2 nm. A bázisok síkja a tengelyre merőleges, de a bázisok
egymáshoz viszonyítva 36o-kal elfordulnak, a köztük lévő távolság
0,34 nm. A csavarlat egy-egy 360º-os fordulata között tehát 10 nukleotid
található, a csavarulat távolsága pedig 3,4 nm. Az ettől eltérő tekeredés a
túltekeredés (supercoiling), amely lehet negatív és pozitív.
(→DNS-túltekeredés).
A két szálú DNS állékonyságában jelentős szerepe van a víztaszító hatásnak: A bázisoknak viszonylag nincs töltésük (víztaszítók), a foszfát pedig negatív töltésű (vízkedvelő), ezért kerül a foszfátot tartalmazó gerinc a DNS felszínére, és zárja be a bázisokat. A foszfát miatt a DNS felszíne negatív töltésű, és mert vizes közegben a töltéssel bíró (vízkedvelő) molekulák fordulnak a víz felé, a foszfát akadályozza, hogy a víz hozzáférjen az észterkötéshez, és felbontsa. A foszfátcsoport tehát védi a DNS-t a vízoldékonyságtól. A DNS szerkezetének állandóságában lényeges még az is, hogy a bázisok oxoformában vannak – ez teszi lehetővé, hogy a törzsfejlődésben bekövetkezhessenek szerkezetváltozások. Az enolforma kivételesen fordul elő. A kettős szál biztonságát még az is segíti, hogy a bázisok között jelentékeny London-féle kölcsönhatások is kialakulnak.
A DNS-szálak egymás köré tekeredése végbemehet jobbra és balra is, ezért jobbmenetes (a-, b-, és cDNS) és balmenetes (zDNS) csavarulat is keletkezhet. A bDNS-t (B-form DNA) tekintjük a DNS élettani formájának, a szervezetben általában ez fordul elő. Az aDNS és a cDNS környezeti hatásokra (alacsony nedvesség és sótartalom) a bDNS-ből keletkezik. Az aDNS-ben a bázispárok nem merőlegesek a kettős szál képzelt tengelyére – attól 19o-kal eltérnek –, aminek következtében a kis árok szinte eltűnik, a DNS megrövidül. Egy-egy menetnek megfelelően nem 10, hanem 11 nukleotid helyezkedik el. A cDNS a bDNS-től abban tér el, hogy benne egy-egy csavarulatot 9 nukleotid képez.
A zDNS nevét cikkcakkos (zig-zag) felcsavarodásáról kapta, amely a nukleozidok térbeli elhelyezkedéséből keletkezik. Szemben az anti helyzetű a- és bDNS-sel, a zDNS-ben a pirimidin- anti, a purinnukleozidok szün helyzetűek, ezért bennük csak egyféle árok található. Egy-egy csavarmenetet 12 nukleotid képez. A zDNS hosszabb és vékonyabb, mint a bDNS. Előfordul, hogy a DNS-nek csupán egy-egy rövidebb szakaszán alakul ki.
A két szálú DNS jóval állékonyabb, mint az egyszálú, mert a kettős csavarodás védi a bázisokat a károsító, másulást okozó vegyi és enzimhatásoktól. Erre utal pl. az is, hogy a citidin deaminacioja, aminek következtében a citidinből uracil keletkezik, csak az egyszálú DNS-en következik be, a kétszálun nem. További előnye a kettős szerkezetnek, hogy ugyanazt a genetikai üzenetet a sejt két szálon is tárolja; a szálak egymás kiegészítői. Ha hiba keletkezik, a nukleotidsor a másik szálról teljesen helyreállítható.
A kettős szerkezet rugalmas, a DNS-folyamatokban, pl. génátíródás, DNS-másolódás vagy DNS-javítás, a két szál szétválik, a folyamatokban résztvevő fehérjék csak így férhetnek a bázisokhoz. A szálak szétválasztását a a DNS-helikázok végzik a hidrogénkötések felbontásával ATP-energia segítségével.
DNS-kettőződés DNA replication a DNS egészének lemásolása a sejt osztódása előtt, azért, hogy a számtartó sejtosztódásban mindkét utódsejtbe teljes DNS állomány kerüljön. A kettőződés csupán néhány órát vesz igénybe, melynek végeztével – átmenetileg – egy olyan sejt keletkezik, amelyben kétszer annyi DNS van, mint a megkettőződést megelőzően (4n, azaz négykészletes sejt). A 4n DNS állomány fele adódik át az osztódásban keletkező két leánysejt mindegyikébe, így a szülő- és leánysejtek – elviekben – genetikailag azonosak lesznek. A DNS-kettőződés meglehetősen pontos: 109 nukleotid lemásolására esik 1 hiba.
DNS-kettőződés és a kromatin átalakulása A DNS kettőződésének a kettőződési villákban szigorúan összhangban kell lennie a buborékban végbemenő kromatin átalakulásával. A DNS-szálak másolódásához a DNS-láncnak el kell válnia a magtestecs hisztonmagjától, ami a magtestecs felbomlásával következik be. A magtestecsek, illetve hisztonok kikerülnek a kettőződési villából, hogy ne akadályozzák a kettőződést. A kettőződést követően, tehát a villa záródásakor azonnal helyre kell állítódnia a kromatinnak. A szabaddá vált hisztonok beépülnek az új megtestecsekbe. Ugyanakkor új hisztonok sokasága is képződik; ezek szintén az új magtestecsek alkotói. Az új hisztonok szintén az S-szakaszban keletkeznek. Az új DNS-láncokhoz azonnal kapcsolódnak a hisztonok, létrehozva az új magtestecseket. Az újonnan képződött hisztonok a késlekedőszálat, az eredeti hisztonok a vezetőszálat tartalmazó DNS-lánchoz kötődnek.
Mint már tárgyaltuk, a magtestecseknek lényeges szerepe van a DNS-kettőződés folyamatának elindításában. A H4 hiszton 20-as lizinjének metilezése, valamint az 5-ös és 12-es lizinjének acetilezése lényeges az előkettőződési össztes kialakításában. Az újonnan képződött H3 és H4 is acetilezett állapotban van az új magtestecs kialakítása előtt.
DNS-kettőződés és a sejtkör A kettőződés az S-szakaszban megy végbe, 6–8 óra alatt. Előkészítése azonban már a sejtosztódás végén az M-szakaszban és a G1-szakaszban elkezdődik a kettőződési előössztes kialakulásával.
DNS-kettőződés folyamata Magsejtűekben, a DNS sok tízezer pontján (kezdőpont) indul egyszerre, de soha nem az egyenes szálú DNS végéről. Ha a kettőződés egy ponton indulna, nem férne bele a másolódáshoz rendelkezésre álló 6–8 órába.
A másolódás kezdőpontjai a DNS-szál pontosan meghatározott helyei, jellemzően ismétlődő, rövid bázissorok, amelyek könnyen szétválnak, és képesek bizonyos fehérjék megkötésére. Tevékenységük pontosan ellenőrzött, a →kettőződési előössztes (prereplicative complex) által. A folyamat négy szakaszra bontható.
DNS-kettőződés folyamatának kezdeti lépései egyetlen kettőződési buborékban Ábra mutatja vázlatosan
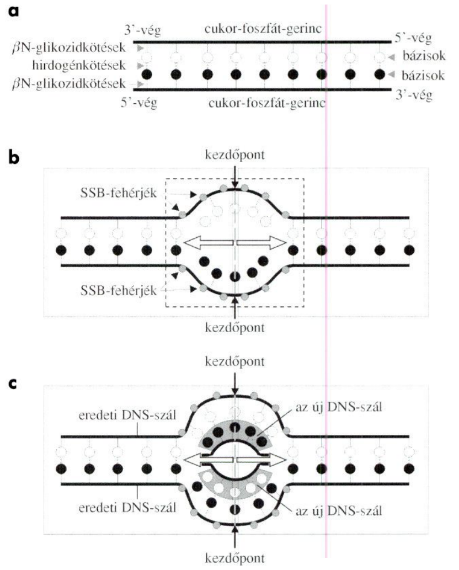 a. Az eredeti
DNS-szál, az egyszerűség kedvéért kiegyenesítve. A vastag vízszintes vonalak a
dezoxiribózok foszfátészterekkel összekötött láncolatát, a
cukor-foszfát-gerincet jelölik. A fekete és fehér karikák a bázisok jelei. A
könnyebb azonosításért az egyik DNS-szálon elhelyezkedő bázisokat a ○ karikák,
a másikon lévőket a ● karikák ábrázolják. A karikák tehát nem utalnak arra,
hogy milyen fajta (adenin, timin, guanin vagy citozin) bázisról van szó.
Látható, hogy a cukor-foszfát-gerinc ellentétes irányban – az egyik 5’–3’ a
másik 3’–5’ helyzetben – a DNS-molekula külső felszínén helyezkedik el, a
bázisok egymással hidrogénkötésekkel, a gerinchez pedig βN-glikozidkötéssel
kapcsolódnak.
a. Az eredeti
DNS-szál, az egyszerűség kedvéért kiegyenesítve. A vastag vízszintes vonalak a
dezoxiribózok foszfátészterekkel összekötött láncolatát, a
cukor-foszfát-gerincet jelölik. A fekete és fehér karikák a bázisok jelei. A
könnyebb azonosításért az egyik DNS-szálon elhelyezkedő bázisokat a ○ karikák,
a másikon lévőket a ● karikák ábrázolják. A karikák tehát nem utalnak arra,
hogy milyen fajta (adenin, timin, guanin vagy citozin) bázisról van szó.
Látható, hogy a cukor-foszfát-gerinc ellentétes irányban – az egyik 5’–3’ a
másik 3’–5’ helyzetben – a DNS-molekula külső felszínén helyezkedik el, a
bázisok egymással hidrogénkötésekkel, a gerinchez pedig βN-glikozidkötéssel
kapcsolódnak.
b. A DNS megkettőződése a kettőződési buborék (kerettel jelölve) kialakulásával kezdődik. A kezdőpontoknál (nyíllal jelölve) a két DNS-szál folyamatosan szétválik. Az átmenetileg egyesszálú DNS-szálakat az SSB fehérjék (single-strand-binding-proteins) rögzítik (vékony nyilakkal jelölve); az eredetileg kiegészült, egyesszálú DNS ugyanis, könnyen újra kettősszálú molekulává egyesülhet. A komplementer bázisok közötti hidrogénkötések felszakadásával a két minta DNS-szál eltávolodik egymástól, az így létrejövő szerkezetet nevezzük kettőződési buboréknak.
c. A hidrogénkötések felszakadását követően megindul az indító RNS-minta keletkezése, majd röviddel ezt követően az új DNS-szálak képződése. A folyamat az eredeti DNS-szálak mentén – azoktól védve –, a felnyílt, eredeti DNS-szálak bázissorrendének megfelelően halad. A folyamat egyszerre zajlik mindkét DNS-szálon. Ahol új DNS képződött, már nem kettő, hanem négy DNS-szál van jelen. Látható, hogy az egyik eredeti DNS-szálon képződő új DNS-szál bázissorrendje azonos a másik oldali eredeti minta DNS-szál bázissorrendjével (a ○-val jelölt eredeti DNS-szálon képződő, ●-val jelölt új DNS-szál teljesen azonos az alsó ●-val jelölt DNS-szállal). A kezdőponttól a DNS-szál szétválása és az új DNS-szálak képződése mindkét irányba halad (⇒ jelöli), aminek következtében két, egymással szemben elhelyezkedő, többé-kevésbé Y alakú képződmény, az úgynevezett kettőződési villák (replication forks) jönnek létre (vonalas téglalapokkal jelölve).
DNS-kettőződés folyamatának kezdeti lépései kiterjedten A fenti történések a DNS egészén egyszerre mennek végbe. Az ábra ezt mutatja, szintén vázlatosan.
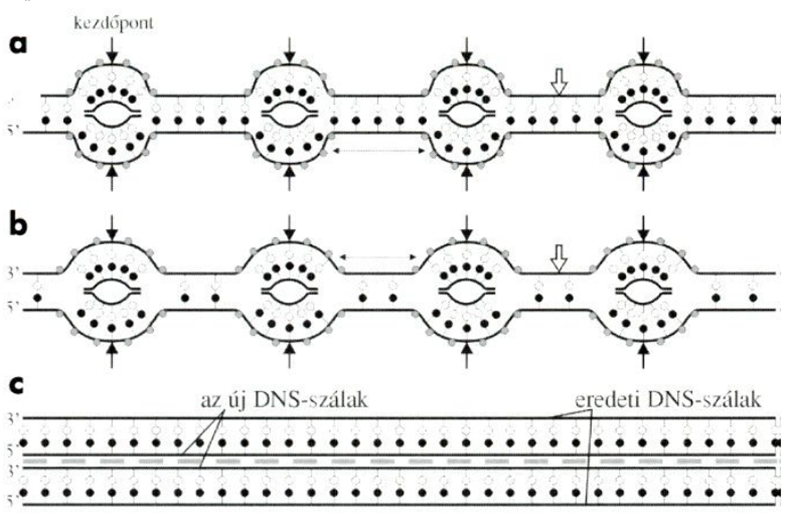
a. A DNS-kettőződés egyszerre több kezdőpontról (nyilakkal jelölve) indul el, és – mint a vázlatos rajz mutatja – egyszerre több kettőződési buborék keletkezik, egymástól a DNS-szál eredeti szakaszaival elválasztva.
b. A DNS-másolódás folyamatosan halad előre, aminek következtében a kettőződési buborékok mindig nagyobbak lesznek, a köztük lévő eredeti DNS-szakaszok (vékony nyilakkal jelölve) hossza pedig rövidül. Az eredeti DNS-szál tehát egyszerre csak rövid DNS-szakaszok átmásolására alkalmas hosszúságon válik ketté, az új DNS-szálak pedig csak a szétnyílásoknak megfelelően képződhetnek
c. A DNS-kettőződés befejező állapota. Az új DNS-szálak kialakultak, a kettőződési buborékok eltűntek. Az Az eredeti DNS-szál és a rajta képződött új DNS-szál ellentétes (5’–3’, illetve 3’–5’) elhelyezkedésű, és az új DNS-szál bázissorrendje azonos azzal az eredeti DNS-szállal, amelyiken a másik új DNS-szál képződött. Két újonnan képződött kettősszálú DNS molekula keletkezett (szaggatott vonallal elválasztva), mindegyikben egy eredeti és egy új DNS-szál van. Az eredeti és a róla másolódott új DNS-szálat tartalmazó DNS-szálat nevezzük kromatidának, a keletkezett két kromatidát pedig testvérkromatidáknak.
A DNS-szálak másolódásával egyidejűleg új magtestecsek formálódnak, amelyekre az új DNS-szálak rögvest rátekercselődnek.
DNS-kettőződési ártmány (kettőződési ártmány)* DNA replication stress a DNS kettőződését nehezítő külső vagy belső károsító hatás. Ilyen ártóhatás a szabálytalan nukleotidbeépülés, a rendellenes DNS-szerkezet, a törékenyhely, a kromatineltérés, a daganatgéntúlzás, a kettőződési fehérjék zavara, valamint külső károsító hatások. A kettőződési ártmány kialakulásának egyik kulcsszereplője a FHIT gén, amelyik a FRA3b gyakori törékenyhelyen (CFS FRA3B) van. Működéskiesése önmagában megzavarja a kettőződési szálágazást.
A kettőződési ártmány olyan sejtállapotot hoz létre, amelyet a kettőződési szálágazás lassulása jellemez, aminek következtében megtorpanhat a DNS-szál kettéválása (fork pausing), egyenlőtlenné válhatnak a testvérágak (sister fork asymmetry), vagy ingataggá válhat a folyamat (increased fork instability). Ha a kettőződési ártmány kifejezett, avagy a DNS törékeny (törékenyhelyek), megállhat a szálágazás (fork stalling), és ha az ATM és ATR nem állítja helyre, a szálágazat összeesik (fork collapse), DNS-hiba keletkezik. A DNS-kettőződési ármány egyik legsúlyosabb következménye a DNS-ingatagság.
DNS-kettőződési hibák és javításuk A DNS-kettőződésbe hiba csúszhat: előfordulhat például, hogy nem kiegészítő bázis épül be, vagy kevesebb, avagy éppen több, aminek következtében hibás DNS keletkezik. Messze a leggyakoribb a nem megfelelő pár kapcsolódása.
A polimeráz rendkívül pontosan másol, nagyjából 100 000 másolásra esik 1 hiba, ami sejtosztódásonként 120 000.
A kettőződésben keletkező hibák egy részét a kettőződési DNS-polimerázok (replicative DNA polymerases) észlelik, az exonukleáz tevékenységgel azonnal kivágják, új nukleotid beépítésével javítják. A javításnak ezt a formáját hibaellenőrzésnek (proofreading) nevezik. A kettőződési hibák 99%-a így kijavítódik. A DNS-kettőződés tehát nagyon pontos. A még maradt 1–2%-nyi hibát, a sejt a párhibajavító enzimrendszer segítségével hozza helyre a kettőződést követően.
Ha a hibát a párhibajavító rendszer sem állítja helyre, másulásként marad meg és adódik tovább a következő sejtnemzedékeknek. Például az eredeti DNS-ben C társul G-vel, amely kettőződési hiba következtében C–A társulássá alakul. A következő kettőződésnél a C–A-t tartalmazó DNS lesz a mintaszál. A C bázis G-vel fog társulni, az eredeti DNS-szál keletkezik. Az A bázis viszont T-vel, egészen más bázispár kerül az eredeti (C–G) helyére.
DNS-kivágás az egyik DNS-szál (általában az 5’-végű) exonukleáz általi eltávolítása a DNS végéről.
DNS-kötő fehérjék DNA binding proteins a DNS-hez elektronkötéssel kapcsolódó fehérjék; ezek alakítják ki a kromoszómák térszerkezetét, formálják, szabályozzák a DNS-t. Sajátos gomolyokkal (DNS-kötő gomolyok) fűződnek a DNS-hez. Legtöbbjük →cinkujj gomolyokkal kapcsolódik, pl. TF3A-ban 37 ilyen gomoly kapcsolódik egymáshoz hajlékony szálakkal; ezek 37, 4–12 nukleotidnyi helyen fűződnek a DNS-hez. Sokféle DNS-kötő fehérje ismert: →CTCF, →TF3A, →ZiF268
DNS-kötő gomoly DNA binding domain a DNS-hez kötődő gomoly. (→fehérjegomoly)
DNS-kötő gomolyok DNA binding domains, DBDs a DNS 4–12 bázispárnyi szakaszával fajlagosan kötődő gomolyok. A DNS-kötő fehérjéket ezek alapján csoportosítjuk. Többféle mintázatúak, pl. előfordul bennük:
▪ cinkujj* mintázat (zinc finger motif) 25 aminosavnyi ujjszerű hurokmintázat, amelyben négy állandó aminosav (két cisztein, két hisztidin) két cinkiont köt; ezek ismétlődnek egymás után.
▪ α-csavarodás–hurok–α-csavarodás* mintázat (helix-loop-helix motif) hurokelemmel lazán összekötött, egymást fedő α-csavarodások;ez a leggyengébb kapcsolásmintázat.
▪ leucinos zármintázat* (leucine zipper motif) kétfordulatú csavarmenetszerű aminosavsor, amelyben minden hetedik aminosav leucin; ez ismétlődik mindkét fordulatban.
▪ α-csavarodás–fordulás–α-csavarodás* mintázat (helix-turn-helix motif) rövid kapcsolóval összekötött, DNS-fajlagosan összekapaszkodott két α-csavarodás. Stb.
bZIP gomoly (basic leucine zipper domain) víztaszító leucinben és lizin–argininben gazdag felismerő részeket tartalmaz – az előző a kettőződést, az utóbbi a DNS-hez kapcsolódást hozza létre.
cinkujj gomoly* zinc-finger domain több, ujjszerű alakulatot (cinkujj mintázat) tartalmaz; képes az RNS-sel is társulni.
MYB (vírusfehérje [avian myelo blastomatosis virus] nevéből származik) a kromoszómák végrészének kétszálú DNS-éhez fajlagosan kapcsolódó gomoly; a GGTTAG/CCAATC mintázatot ismeri fel.
DNS-ligáz DNA ligase a dezoxiribonukleotidokból felépülő töredékszakaszokat (DNS-kettőződésben az Okazaki-töredékeket) – a bázishiányok kitöltése nélkül –, energia (ATP) felhasználásával kapcsolja össze egyetlen foszfodiészter-kötéssel. Ezzel az új DNS-szál folyamatossá válik, a hiányosságok megszűnnek. Az enzim az 5’-foszfát (5’-P) és a 3’-OH között alakítja ki a kötést; az 5’-dRP-vel (5’-dezoxiribóz-foszfát) nem hoz létre kötést. (→Okazaki-töredékek)
DNS-ligáz-1 (LIG1) A báziskivágó javításban és a DNS-kettőződésben vesz részt.
DNS-ligáz-3α (LIG3α) A báziskivágó javításban vesz részt a sejtmagban és az energiatestecsben is (mitokondrion)
DNS-másulás DNA mutation
(mutáció) az emberi örökítőanyagban bekövetkező vegyi módosulás. Ezek a
módosulások érinthetik az örökítőanyag kódoló és nem kódoló szakaszait
egyaránt, jellemzően, de nem kizárólag (irányított másulás), véletlenszerűek,
és lehetnek maradandóak, avagy időlegesek. A másulás járhatnak az örökítőanyag
bázissorrendjének megváltoztatásával, de létrejöhetnek olyan vegyi
változásokkal is, amelyek a bázissorrendet alapvetően nem befolyásolják (átírásirányító
változások).
(Az egyetlen bázisra vonatkozó változást pontmásulásnak* [point mutation], egynukleotidos változásnak [single nucleotide variation; SNV] és egybázisú sokalakúságnak* [single nucleotide polymorphism, SNP] is nevezik.)
A DNS változásának több formája ismert:
▪ nukleotidcsere/báziscsere (single nucleotide variation, SNV). (→bázispárcsere)
▪ nukleotidtöbblet, nukleotidvesztés (insertion, deletion). (→bázistöbblet és bázisvesztés)
▪ részkettőződés, amely valamely DNS-szakasz kétszereződése, többszöröződése.(→részkettőződés)
▪ részhiány, amely valamely nagyobb DNS-szakasz törlődése.
▪ ismétletbővülés, amely az ismétletek, legtöbbször a mikroismétletek rendellenes többszöröződése. (→ismétletbővülés)
A DNS-másulás hatása szerint beszélünk:
▪ DNS-eltérésről*, amely betegséget, fejlődési rendellenességet nem okozó DNS-másulás. Lehet:
- néma DNS-eltérés*, amelyben megváltozott RNS és/vagy fehérje nem keletkezik;
- változtató DNS-eltérés*, amelyben keletkezik megváltozott RNS és/vagy fehérje.
▪ DNS-csorbáról*, amely betegséget, fejlődési rendellenességet okozó DNS-másulás.
A DNS-másulás keletkezése szerint megkülönböztetünk:
▪ Örökletes (csírasejtes) DNS-másulást* (germline [hereditary] mutation), ami a csírasejtben lévő báziseltérés. A szülők valamelyikétől (a pete- vagy az ondósejtből) öröklődik, és jelen van az utód mindegyik sejtjében.
▪ Szerzett (testi) DNS-másulást* (acquired [somatic] mutation), ami a személy életében keletkező géneltérés; csak néhány sejtben – amelyekben kialakult, és amelyek azokból származnak – van jelen, nem adódik tovább az utódokba.
A DNS-beli helye szerint lehet →génmásulás, ismétletmásulás.
DNS-metilezés DNA methylation metilcsoport (CH3) elektronkötése a DNS citozinjának 5-ös szénatomához – 5-metil-citozin keletkezik. A metilcsoportot a DNS-metil-transzferáz csatolja az S-adenozil-metioninról. A metilcsoport majdnem mindig ahhoz a citozinhoz kapcsolódik, amelyet guanin követ; ezt nevezzük CpG-helynek (→CpG-sziget) – írják mCG (methylation of cytosine followed by guanin) formában is. A CpG nukleotidkettősök az emberi nukleotidlánc 1%-át teszik ki; 70–80%-uk metilezett.
A citozin metilezése a génműködés szabályozásának törzsökös formája, meghatározóan befolyásolja a génátíródást. Mivel a génen kívülről szabályozódik, epigenetikai szabályozásnak nevezzük. Jelentősen változik az egyedfejlődés idején, majd állandósul. Fontos szerepe van a sejtnövekedés, a sejtelkülönülés, az érképződés, a DNS-hiba javításának irányításában, az X-kromoszóma némításában (X chromosome inactivation), a genomlenyomatban (genomic imprinting), az embrionális szövetek kialakulásában stb.
Az indító (promoter) környéki metilezés gátolja a génátíródást, a gén némává válik – ez a terület gazdag CpG-szigetekben és más átírásfehérje-kötőhelyekben. A génen belüli metilezés (gene body methylation) serkenti az átíródást, és gátolja az átíródás meghibásodását. A fokozó (enhancer) metilezésének jelentősége bonyolultabb, valószínűleg nemcsak az átírásfehérje kapcsolódásával függ össze.
Az olyan citozin metilezését, amelyet adenin (A), citozin (C) vagy timin (T) követ (tehát nem guanin), nem CpG-metilezésnek nevezzük, szokásosan CpH vagy mCH formában írjuk (H = A, C vagy T). Ez az őssejtekben (ébrényi sejtekben) és az idegsejtekben (neuronokban) fordul elő.
A DNS metilezését a TET1, TET2, TET3 (ten-eleven translocation) enzim ellensúlyozza: ezek az enzimek oxidálják az 5-metil-citozint. A metilezéses szabályozáshoz tartoznak még az „olvasó” fehérjék (reader proteins), amelyek a metilezett DNS-hez kapcsolódnak, és kromatint alakító fehérjéket és fehérjeösszleteket toboroznak. Ilyenek a methyl-CpG binding domain fehérjék (MBD fehérjék) és bizonyos átírásfehérjék.
A DNS metilezés kétféleképpen befolyásolhatja a gén működését: meggátolja, hogy az átírásfehérje kapcsolódjék hozzá, de talán még fontosabb az MBD-fehérjék kötése: az MBD-fehérjék ugyanis további fehérjéket, mint hiszton-deacetiláz és más kromatinformáló fehérjét kapcsolnak, amelyek befolyásolják a hisztonokat, és tespedt kromatinok (heterokromatinok) keletkeznek.
A CpG kettősök csökkent metilezettsége (hypomethylation) a folyamatos génátíródáshoz vezet (géntúlműködés), fokozott metilezettsége (hypermethylation) pedig alulműködéssel jár.
A DNS metilezési zavarai összefüggnek sokféle betegséggel, reumás és idegbetegségekkel, valamint a rákokkal is. A rákoknál összességében csökken a metilezés a genomban (általános alulmetilezés), egyes szabályozó gének területén viszont fokozott (túlmetilezés).
Mivel a ráksejtek és az ép sejtek metilezése eltér, a metilezés formája lehet daganatjelző, pl. a SEPT9 gén fokozott metilezése jellemző a vastagbélrákokra. Az emberi sejtekben jóformán csak a citozin metileződik, nagyritkán azonban az adenin is: N6-metil-adenin keletkezik. Ez is gátolja a génkifejeződést, főleg az X kromoszómákhoz kapcsolt géneknél. Fontos szerepet tulajdonítanak neki az ébrényi és a magzati fejlődésben.
DNS-metil-transzferáz (DNA methyltransferase, DNMT) fehérjecsalád, amelynek három tagja, a DNMT3A, DNMT3B és a DNMT1 metilezi a DNS-t. A DNMT3A és 3B főleg a korai fejlődés szakaszában működik, a sejtosztódások S-szakaszában leginkább az DNMT1 tevékenykedik. DNS-metil-transzferáz a metilcsoportot DNS citozinjának 5-ös szénatomjához csatolja az S-adenozil-metioninról, és 5-metil-citozin keletkezik. (→DNS-metilezés)
A metilcsoportot a ten-eleven translocation (TET) enzimcsalád három tagja, TET1, TET2 és TET3 távolítja el: elektront von el az 5-metil-citozinból. A TET és a DNMT fehérjék szerkezete nagyon hasonló, ezért nevezik őket DNS-metilező íróknak és törlőknek (DNA methylation writers, erasers).
DNS-mintázatok DNA motifs másodlagos DNS-szerkezetek (non-B-DNA structures). A DNS elsődleges, kettős csavarodású szerkezetétől (B-DNA) eltérő DNS-alakzatok (észleletek); az átírásfehérjék ezek alapján ismerik fel kapcsolódási helyüket. Szerepük meghatározó számos sejtfolyamatban: génkifejeződés, DNS-kettőződés, DNS-átrendeződés, immunválasz, végrészek megtartása. Gyakran keletkezik bennük hiba; másulásuk betegséghez vezethet. Sok és sokféle DNS-mintázat fordul elő: E-doboz, G-négyes, i-mintázat, DNS-hármas (DNA-triplex), zDNS és a DNS-kereszt (DNA-cruciform).
DNS-polimeráz (POL) DNA polymerase DNS-t képező enzim. Megkülönböztetünk DNS-függő és RNS-függő DNS-polimerázt. Az előbbi a DNS-t, az utóbbi az RNS-t használja mintafelületként.
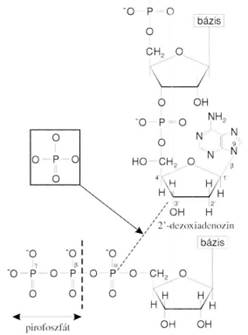 DNS-függő DNS-polimeráz DNA dependent DNA polymerase kettős
hatású: a nukleozid 5’-trifoszfát α-helyzetű foszfátját köti a nukleotidlánc
végét képező 3’-OH csoporthoz diészterkötéssel, másrészt 3’→ 5’ exonukleáz
hatású. Minden új nukleotid beépítése előtt ellenőrzi a legutolsót, és ha nem
megfelelő, kivágja, majd beépíti helyette a megfelelőt. A polimeráz csak a
3’-OH-csoporthoz képes kapcsolódni, egyébként nem tevékeny. A kapcsolódás tehát
5’→ 3’ irányú, fordítva (3’→ 5’ irányban) nem jön létre. Eközben a nukleozid
5-trifoszfát α és β jelzésű foszfátja közötti kötés vízelvonás mellett
felszakad, a β és γ jelzésű foszfátot tartalmazó pirofoszfát szabaddá válik. Az
emberi DNS-polimerázok mindig csak a már meglévő nukleotidlánchoz kapcsolnak
újabb nukleotidot, két szabad nukleotidot nem képesek összekötni. A báziskivágó
javításban a POLβ, POLδ/ε és a POLλ, a párhibajavításban a POLβ, POLε vesz
részt
DNS-függő DNS-polimeráz DNA dependent DNA polymerase kettős
hatású: a nukleozid 5’-trifoszfát α-helyzetű foszfátját köti a nukleotidlánc
végét képező 3’-OH csoporthoz diészterkötéssel, másrészt 3’→ 5’ exonukleáz
hatású. Minden új nukleotid beépítése előtt ellenőrzi a legutolsót, és ha nem
megfelelő, kivágja, majd beépíti helyette a megfelelőt. A polimeráz csak a
3’-OH-csoporthoz képes kapcsolódni, egyébként nem tevékeny. A kapcsolódás tehát
5’→ 3’ irányú, fordítva (3’→ 5’ irányban) nem jön létre. Eközben a nukleozid
5-trifoszfát α és β jelzésű foszfátja közötti kötés vízelvonás mellett
felszakad, a β és γ jelzésű foszfátot tartalmazó pirofoszfát szabaddá válik. Az
emberi DNS-polimerázok mindig csak a már meglévő nukleotidlánchoz kapcsolnak
újabb nukleotidot, két szabad nukleotidot nem képesek összekötni. A báziskivágó
javításban a POLβ, POLδ/ε és a POLλ, a párhibajavításban a POLβ, POLε vesz
részt
DNS-polimeráz-α (POLα) DNA polymerase alfa (DNA Pol α) a primáz enzimmel együttesen a késlekedő DNS-szál darabjait építi.
DNS-polimeráz-β (POLβ) DNA polymerase beta (DNA Pol β) a legkisebb polimeráz (39 kDa, 335 aminosav). Két gomolya van: a DNS-t képző polimeráz gomoly és a dezoxiribóz-foszfátot hasító liáz gomoly. Nincs benne a 3’→ 5’ keretolvasó exonukleáz. A polimeráz-X családba tartozik. Részt vesz a DNS-hiba báziskivágó javításában. (→DNS-hibák)
DNS-polimeráz-γ (POLγ) DNA polymerase gamma (DNA Pol γ) az energiatestecs (mitochondrion) DNS-ének képzésében vesz részt.
DNS-polimeráz-δ (POLδ) DNA polymerase delta (DNA Pol δ) negytagú enzimössztes: a DNS kettőződésében a vezetőszálat és a késlekedőszálat képezi. A négy alegysége a POL1, POL2, POL3 és a POL4, amelyeket a POL1, POL2, POL3, illetve a POL4 kódol.
DNS-polimeráz-ε (POLε) DNA polymerase epsilon (DNA Pol ε) törzsökös, négyegységes enzim, képezi a vezetőszálat, részt vesz a DNS-hiba báziskivágó javításában. (→DNS-hibák)
DNS-polimeráz-λ (POLλ) DNA polymerase lambda (DNA Pol λ) a DNS-hiba báziskivágó javításában vesz részt. (→DNS-hibák)
RNS-függő DNS-polimeráz RNA dependent DNA polímerase az RNS-ről képez DNS-t. Szokványos néven fordított transzkriptáz.
DNS-sokalakúság* DNA polymorphism valamely népesség legalább 1%-ában előforduló DNS-változat. (→sokalakúság)
DNS-szabályozók a DNS működését irányító molekulák. Két csoportot, a DNS-ben lévő és a DNS-en kívüli szabályozókat különböztetjük meg. Az előbbiek a DNS-beli szabályozók (cis-acting regulatory elements, CREs), a szabályozó bázissorok. (→DNS-elemek) Az utóbbiak a bázissor-szabályozók (trans-acting regulatory elements, TREs, epigenetic regulators) a bázissorok tevékenységét irányító molekulák; nem változtatnak a bázissorokon. (→bázissor-szabályozás)
DNS-szál DNA strand a DNS egyik fele: nukleotidok (dezoxiribózok, foszfát és bázis) foszfodiészter-kötéssel kapcsolódott hosszú sora. Két DNS-szál gyenge kötésekkel egymás köré tekeredve alkotja a DNS-t. A DNS-folyamatokban a két szál átmenetileg elválik; feladatuk szerinti megkülönböztetésükre más az elnevezésük. A génátírásban azt a DNS-szálat, amelynek bázissorrendje megegyezik az RNS bázissorrendjével, kódoló vagy pozitív (sense, értelmes) szálnak nevezzük, a mintául szolgáló pedig a negatív (antisense, értelmetlen) szál. Ez utóbbi másolódik, ezért mintaszálnak is mondjuk. A kódoló DNS-szál a másolódott szál, vagyis az RNS. A DNS-kettőződésben a másolódó, vagyis a minta DNS-szálat szülői, a másolódott szálat pedig leány DNS-szálnak nevezzük.
DNS-szálak képződési folyamata a kettőződési villákban megy végbe.
● Másolás a DNS-polimeráz végzi.
▪A polimeráz a már meglévő nukleotidsor 3’-végi OH-csoportjához képes nukleotidot kötni. Tehát kettőződés mindenkor 3’-végen kezdődik, és halad az 5’-vég felé.
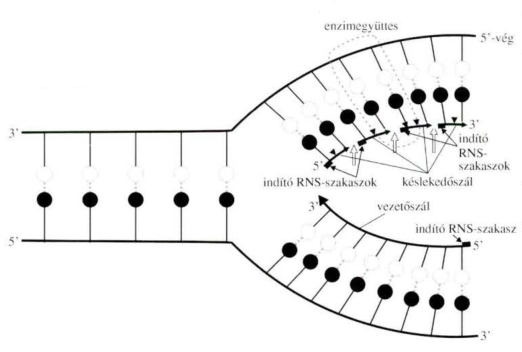 ▪ A DNS-polimeráz a nukleotidánchoz nem tud
kapcsolódni, mert szabad 3’-OH csoportra van szüksége. A primáz egy
RNS-polimeráz viszont képes elkezdeni a nukleatin kapcsolást, és rövid (5–20 bázisnyi)
RNS-vezetőszálat (primer) hozz létre. A DNS-polimeráz-α meghosszabbítja az
RNS-indítószálat 20 nukleotiddal. Ezt követően vezetőszálat a DNS-polimeráz-E,
a késlekedőszálat a DNS-polimerz-D képezi tovább az 5’- vég felé.
▪ A DNS-polimeráz a nukleotidánchoz nem tud
kapcsolódni, mert szabad 3’-OH csoportra van szüksége. A primáz egy
RNS-polimeráz viszont képes elkezdeni a nukleatin kapcsolást, és rövid (5–20 bázisnyi)
RNS-vezetőszálat (primer) hozz létre. A DNS-polimeráz-α meghosszabbítja az
RNS-indítószálat 20 nukleotiddal. Ezt követően vezetőszálat a DNS-polimeráz-E,
a késlekedőszálat a DNS-polimerz-D képezi tovább az 5’- vég felé.
▪ A másolódott DNS, mivel kiegészítője a mintaszálnak, az iránya fordított, vagyis a mintaszál 3’-végénél lesz az 5’-vége.
▪ A 3’ → 5’ irányú DNS-szálon a másolódás iránya azonos a szál irányával és a villa nyílásának irányával is. Ez azt jelenti, hogy elegendő egyetlen ks RNS-veztő, amely megszakítás nélkül halad, a villa nyílódásával párhuzamosan. Ezt a szálat vezetőszálnak, leadig strand nevezik.
▪ Az 5’ → 3’ irányú szálon a másolódás csak fordítva mehet. Ezen is keletkezik kis RNS-vezető, köti a polimerázt és vezeti a 5’-felé, másolva a DNS-t. A villa azonban nyílik, a polimeráz nem mehet visszafelé, szabad terület marad. Ehhez másik RNS-vezető kapcsolódik, vezetve a polimerázt. Ám a DNS-szálak ellentétes irányú elválásával ismét lesz szabad DNS-szál. Jön újabb RNS-vezető stb. Ez azt jelenti, hogy a DNS szakaszonként másolódik. A szakaszokat Okazaki-töredékeknek nevezzük, a szakaszonként másolódó DNS-szál pedig a késlekedő szál (lagging strand).
▪ A DNS-szakaszokat piciny – egyetlen foszfodiészterkötésnyi – hiányok (nick) (vastag nyilakkal jelölve) választják el. A töredékszakaszok tehát rövid RNS- és rövid (1000–1500 nukleotid) DNS-szakaszból állnak.
● A DNS-szálak összekapcsolása. A töredékszakaszok hossza tehát nem változik; az egyik végükön az RNS-darab lebomlik, a másikon, ugyanilyen hosszú DNS-szakasz képződik. A folyamat eredményeképpen két, hiánnyal elválasztott töredékszakasz van egymás mellett, de ezeket már csak DNS alkotja. A végek foszfodiészterkötéssel kapcsolódnak a DNS-ligáz közreműködésével, energia felhasználással. A kötésekkel a késlekedőszál is folyamatossá válik.
DNS-szerkesztés
genome editing, genome engineering,
gene editing (genomszerkesztés)
a DNS genetikai megváltoztatása: beékelünk, kilökünk, módosítunk vagy cserélünk
egy bázist vagy bázissort az élő szervezet DNS-ébe. A DNS-szerkesztés,
ellentétben a véletlenszerű korai genetikai változtatásokkal célzott, sajátos
helyen történik, például célmolekula előállítására. Egyre inkább a kezelések
megerősítésére szolgálnak, annyira, hogy elterjedt az emberi génszerkesztési
kezelés fogalma is. Feltétlen ez a jövő, a rák kezelésében mindenképp. Jó példa
a használatára a sarlósejtes vérszegénység és a Duchenne-kór; ezeknek a
betegségeknek a génhibái genetikai szerkesztéssel gyógyítjuk, de genetikai
szerkesztést alkalmazunk a CART-T-sejtes kezelésekben is.
DNS-szerkezet
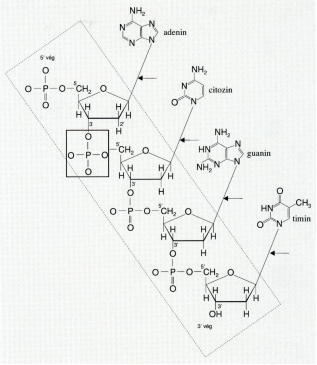 ▪ A DNS-szál szerkezete. A szaggatott vonallal körülzárt területen a
dezoxiribóz molekulák foszfodiészter-kötésekkel kapcsolt sorozata látható – ez
a DNS gerince (dezoxiribózlánc, backbone). A vastag vonallal körberajzolt rész
az egyik foszfodiészter-kötést jelöli; látható, hogy a kötés két dezoxiribóz
egy-egy, a 3’, illetőleg az 5’-szénatomjához kapcsolódik, ezért beszélünk 3’,
5’-foszfodiészter-kötésről (a 3’-szénatom OH-ja egyesül az 5’-szénatom
foszfátjával). (→foszfodiészter-kötés) Az 5’‑szénatomon kapcsolt dezoxiribóz a
3’-szénatomjával kötődik a következő dezoxiribóz 5’-szénatomjához stb.
Értelemszerűen a sorozat két végén a dezoxiribóz csak egy-egy kötéssel
kapcsolódik. A sorozat legfelső (upstream) tagjának 5’-szénatomján foszfát van
– ezt nevezzük 5’-végnek –, a legalsó tagjának (downstream) 3’-szénatomján
pedig OH – 3’-vég. (Nagyon ritkán előfordulhat, hogy az 5’-szénatomon OH
csoport van – a foszforsavval észteresített foszfátcsoport nem alakul ki.) A
foszfátnak és az OH-csoportnak is van töltése, ezért a nukleinsav töltéssel
bíró molekula. A bázisok nem vesznek részt a gerinc kialakításában, kilógnak
belőle; a dezoxiribózokhoz N-glikozidos kötésekkel kapcsolódnak (nyilakkal
jelölve). A gerinc minden eleme egyforma, a hozzájuk kötődő bázisok
sorrendje azonban változó. A DNS leírását 5’→3’ irányban adjuk meg a bázisok
egybetűs betűszóival. Az ábrán látható szakasz: 5’ ACGT 3’ (adenin, citozin,
guanin, timin). A DNS egészében a bázisok (a nukleotidok) milliói egymás
mellett vannak semmi nem választja el őket. A DNS egyes elemeinek (gének,
ismétlete stb.) tisztán tevékenységük szerinti. Az egységek szerkezeti alapon
nem különülnek el.
▪ A DNS-szál szerkezete. A szaggatott vonallal körülzárt területen a
dezoxiribóz molekulák foszfodiészter-kötésekkel kapcsolt sorozata látható – ez
a DNS gerince (dezoxiribózlánc, backbone). A vastag vonallal körberajzolt rész
az egyik foszfodiészter-kötést jelöli; látható, hogy a kötés két dezoxiribóz
egy-egy, a 3’, illetőleg az 5’-szénatomjához kapcsolódik, ezért beszélünk 3’,
5’-foszfodiészter-kötésről (a 3’-szénatom OH-ja egyesül az 5’-szénatom
foszfátjával). (→foszfodiészter-kötés) Az 5’‑szénatomon kapcsolt dezoxiribóz a
3’-szénatomjával kötődik a következő dezoxiribóz 5’-szénatomjához stb.
Értelemszerűen a sorozat két végén a dezoxiribóz csak egy-egy kötéssel
kapcsolódik. A sorozat legfelső (upstream) tagjának 5’-szénatomján foszfát van
– ezt nevezzük 5’-végnek –, a legalsó tagjának (downstream) 3’-szénatomján
pedig OH – 3’-vég. (Nagyon ritkán előfordulhat, hogy az 5’-szénatomon OH
csoport van – a foszforsavval észteresített foszfátcsoport nem alakul ki.) A
foszfátnak és az OH-csoportnak is van töltése, ezért a nukleinsav töltéssel
bíró molekula. A bázisok nem vesznek részt a gerinc kialakításában, kilógnak
belőle; a dezoxiribózokhoz N-glikozidos kötésekkel kapcsolódnak (nyilakkal
jelölve). A gerinc minden eleme egyforma, a hozzájuk kötődő bázisok
sorrendje azonban változó. A DNS leírását 5’→3’ irányban adjuk meg a bázisok
egybetűs betűszóival. Az ábrán látható szakasz: 5’ ACGT 3’ (adenin, citozin,
guanin, timin). A DNS egészében a bázisok (a nukleotidok) milliói egymás
mellett vannak semmi nem választja el őket. A DNS egyes elemeinek (gének,
ismétlete stb.) tisztán tevékenységük szerinti. Az egységek szerkezeti alapon
nem különülnek el.
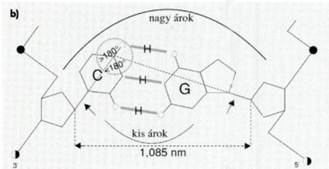
 ▪ A kettős DNS-szál szerkezete. A két DNS-szálat a
bázisok kapcsolják össze hidrogénkötésekkel. A gerinc a DNS külső, a bázisok a
belső részét alkotják. A szemben lévő bázisok egymás kiegészítői (complementary
bases), az egyik purinbázis, a másik pirimidinbázis, vagyis egy egygyűrűs és
egy kétgyűrűs bázis kötődik össze. Kizárólag a kiegészítő bázispárok
kapcsolódhatnak: az egyik DNS-szál adeninje (A) a másik timinjével (T) – A–T
párosodás –, illetve az egyik guaninja (G) a másik citozinjával (C), G–C párosodás.
A kiegészítő bázispárok szigorúan meghatározott társulása egyszerű térbeli
elhelyezkedésükből adódik: csak az egymással szemben lévő adenin és timin,
illetve guanin és citozin kerülnek olyan helyzetbe, hogy köztük hidrogénkötés
alakuljon ki. Az adenin (A) és a timin (T) között két, a guanin (G) és a
citozin (C) között három hidrogénkötés jön létre (H-val jelölve), ezért az
utóbbi erősebb. Kétféle hidrogénkötés (N-H…O, N‑H…N) fordul elő; ezek
kötéstávolsága különböző. A hidrogénkötés térben irányított, akkor a
legerősebb, ha egyenes vonalú. Egyenes vonalúságának megtartása fontos a
csavarulat kialakításában. A DNS-szálak végein egy-egy kötetlen 5’- és
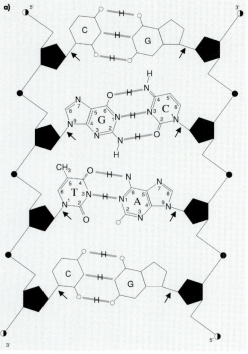
3’-szénatom van. Kinagyított részlet, amelyen jól látható, hogy a szemközti
nukleotidok egymástól pontosan meghatározott távolságra (1,085 nm) vannak, de
nem pontosan szemben, aminek következtében az egymással bezárt szögük az egyik
oldalon nagyobb, a másikon kisebb, mint 180o (szaggatott vonallal
jelölve). A DNS feltekeredett állapotában a nagyobb szögnél nagyobb, a kisebb
szögnél kisebb behúzódás keletkezik. Az előbbit nagy ároknak, az utóbbit kis
ároknak nevezzük.
▪ A kettős DNS-szál szerkezete. A két DNS-szálat a
bázisok kapcsolják össze hidrogénkötésekkel. A gerinc a DNS külső, a bázisok a
belső részét alkotják. A szemben lévő bázisok egymás kiegészítői (complementary
bases), az egyik purinbázis, a másik pirimidinbázis, vagyis egy egygyűrűs és
egy kétgyűrűs bázis kötődik össze. Kizárólag a kiegészítő bázispárok
kapcsolódhatnak: az egyik DNS-szál adeninje (A) a másik timinjével (T) – A–T
párosodás –, illetve az egyik guaninja (G) a másik citozinjával (C), G–C párosodás.
A kiegészítő bázispárok szigorúan meghatározott társulása egyszerű térbeli
elhelyezkedésükből adódik: csak az egymással szemben lévő adenin és timin,
illetve guanin és citozin kerülnek olyan helyzetbe, hogy köztük hidrogénkötés
alakuljon ki. Az adenin (A) és a timin (T) között két, a guanin (G) és a
citozin (C) között három hidrogénkötés jön létre (H-val jelölve), ezért az
utóbbi erősebb. Kétféle hidrogénkötés (N-H…O, N‑H…N) fordul elő; ezek
kötéstávolsága különböző. A hidrogénkötés térben irányított, akkor a
legerősebb, ha egyenes vonalú. Egyenes vonalúságának megtartása fontos a
csavarulat kialakításában. A DNS-szálak végein egy-egy kötetlen 5’- és
3’-szénatom van. Kinagyított részlet, amelyen jól látható, hogy a szemközti
nukleotidok egymástól pontosan meghatározott távolságra (1,085 nm) vannak, de
nem pontosan szemben, aminek következtében az egymással bezárt szögük az egyik
oldalon nagyobb, a másikon kisebb, mint 180o (szaggatott vonallal
jelölve). A DNS feltekeredett állapotában a nagyobb szögnél nagyobb, a kisebb
szögnél kisebb behúzódás keletkezik. Az előbbit nagy ároknak, az utóbbit kis
ároknak nevezzük.
DNS-topoizomeráz (TOP) DNS-t hasító, újraegyesítő enzim. Háromfélét (topoizomeráz-1 [TOP1], topoizomeráz-2 [TOP2], topoizomeráz-3 [TOP3]) ismerünk. Átmenetileg meghasítják a DNS-t, majd, a DNS megfelelő átalakulása után, egyesítik. A törések a kettőslánc egyik (TOP1, 3) vagy mindkét (TOP2) DNS-szálát érinthetik. Ahol törés keletkezik, a DNS alakja és elhelyezkedése megváltozik. Egy DNS-szál megszakadása DNS ernyedést, mindkét szál megszakadása DNS-alultekeredést okoz. A topoizomerázok ezeket a szerkezeti módosulásokat gátolják.
Ténykedésük átmeneti köztes terméke az elektronkötéssel kapcsolódó tirozil-DNS-foszfodiészter (tyrosyl-DNA complex). Ha a topoizomeráz működése gátolt vagy nem megfelelő, a tirozil-DNS-foszfodiészter tirozinja a tört véghez rögzül, és gátolja a DNS működését, másolódását; a sejt elpusztul. A topoizomeráz-1 köztes termékeként keletkező tirozil-DNS-foszfodiészter a 3’-véghez, a topoizomeráz-2 folyamatában keletkező a 5’-P-véghez kapcsolódik (felszaporodva a kettős töréseken rendkívül mérgező). A folyamatot TOP1, TOP2 tyrosyl-DNA cross linkage/link-nek nevezik. Egyéb elnevezés: single strand brake with tyrosyl–DNA covalent linkage; magyarul: TOP1/2 tirozil-DNS-keresztkötés*. Ezeket a keresztkötéseket a tirozil-DNS-foszfodiészterázok (TDP) bontják. A TDP1 a 3’-végen, és alakítja 3’-P végződésűvé, melyet a PNKP (polynucleotide kinase 3’-phosphatase) alakít 3’-OH-vá. Ez azért fontos, mert a DNS-polimeráz csak az OH-csoporthoz képes kapcsolódni. A TDP1 a 3’-foszfoglikolát végződést is bontja, hasonlóan az APE1-hez. A TDP2 az 5’-végen bont, helyreállítja az 5’-P-t.
A topoizomerázok baktériumok létezésében meghatározók, mivel a baktériumok DNS-ét alakítják a létezésüknek negfelelően. Gátlásuk a baktériumok pusztulásához vezet, ezért a topoizomeráz-gátlók hatásosak a bakteriális fertőzések leküzdésében; antibiotikumok.
DNS-válaszelemek* response elements rövid bázissorok egyes gének indítóiban vagy a fokozóiban; fajlagosan kötik a gént serkentő átírásfehérjéket. Gyakran olyan rövid egyenes vagy ellentett ismétletekből állnak, amelyeket változó számú bázispárok választanak el. Jelen kell lenniük ahhoz, hogy a sejt válaszoljon valamilyen ingerre, pl. hormonokra (hormonválaszelemek).
Nagyon sokféle válaszelem ismert:
cAMP response element (CRE); B recognition element; AhR-, dioxin- or xenobiotic-responsive element; hypoxia-responsive elements; hormone response element: estrogen response elements (EREs), androgen response elements (AREs); serum response element (SRE); retinoic acid response elements (RAREs); peroxisome proliferator hormone response elements (PPREs); metal-responsive element (MRE); DNA damage response element (DRE);hormone E-doboz; IFN-stimulated response elements (ISREs); ROR-response element; glucocorticoid response element (GRE); calcium-response element CaRE1; antioxidant response element (ARE); p53 response element; thyroid hormone response element; growth hormone response element (GHRE); sterol response element; polycomb response elements (PREs); vitamin D response element (VDRE); rev response element (RRE) stb.
DNS-változat* a DNS bázissorának csekély mértékben eltérő egyénsajátos formája. A DNS mindenkiben némileg más; jószerivel nincs két teljesen azonos DNS-sű egyed. Ezeket a némileg eltérő DNS-formákat nevezzük DNS-változatoknak. A DNS >99%-ka minden egyedben egyforma.
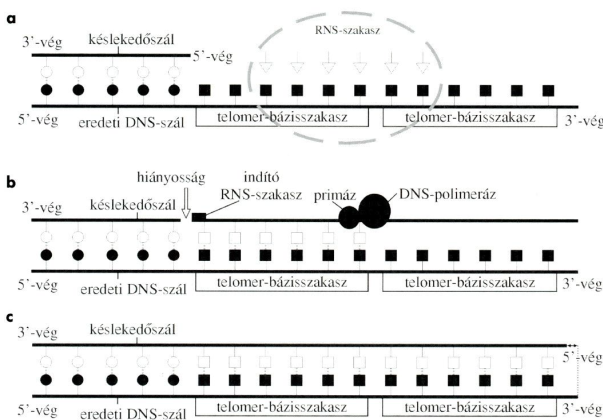 DNS-végrészek másolása A kromoszómavégek, a végrészek (telomers),
hat–nyolc nukleotidos ismétletekből állnak.
DNS-végrészek másolása A kromoszómavégek, a végrészek (telomers),
hat–nyolc nukleotidos ismétletekből állnak.
a. Az újonnan képződött DNS-lánc 5’-vége a késlekedő-, a 3’-vége az eredeti DNS-szál; a szálak egyforma hosszúak. Az utóbbihoz a telomeráz hozzákapcsolt két hatnukleotidos ismétlődő bázissort (végrész-bázisszakaszt) (■ négyzetekkel jelölve). A bázissor a telomerázban lévő RNS bazissorrendje szerinti.
b. A végrész-bázisszakaszok mintafelszínül szolgálnak. A primáz és DNS-polimeráz ennek alapján képezik a késlekedő DNS-szál 5’-végénél az utolsó töredékszakaszt. Ez a töredékszakasz szintén két, hat-hat nukleotidot tartalmazó végrész-bázisszakaszból áll.
c. A töredékszakasz összekapcsolásakor az RNS-nukleáz eltávolítja az indító RNS-szakaszt; a késlekedő DNS-szál – az 5’-végénél – ennyivel rövidebb marad.
A végrészek csak azokban a sejtekben kettőződnek, amelyekben tevékeny telomeráz enzim van jelen. A telomeráz – vagy a telomeráz-működés – szöveteink nagy részében idővel csökken, de néhány sejtformában, mint például a szöveti őssejtekben, az ivarsejtekben vagy a daganatsejtekben folyamatos.
DNS-vezető, RNS-vezető primer (5–20 bázisnyi) RNS/DNS mintafelület, amely kapcsolódik a kiegészítő bázisaihoz, köti és vezeti a polimerázt, például DNS-kettőződéskor. De alkalmazzuk laboratóriumi módszerekben (PCR, polymerase chain reaction), bázispásztázás is.
energiatermecs-DNS (mtDNS) mitochondrial DNA, mtDNA törzsökös, jellegzetesen kis gyűrűs kétszálú DNS, ~16569 bázispárból áll. A DNS két szálának bázisösszetétele más-más, ennek alapján megkülönböztetünk egy könnyű és egy nehéz DNS-szálat (könnyű és nehéz láncnak mondják, de a DNS-szál elnevezés találóbb). A nehézszál több guanint, a könnyű ennek megfelelően több citozint tartalmaz. A két DNS-szál 13-féle, az elektronszállításban és az ATP-termelésben szerepet játszó fehérjét kódol, továbbá kétféle rRNS-t és 22-féle tRNS-t (mitochondrial tRNA, mtRNA); kettőt-kettőt a szerinnek és a leucinnak, és egyet-egyet a többi 18-féle aminosavnak. Ezek a tRNS-ek némileg különböznek a sejtmagi tRNS-ektől. 12-féle fehérje, a 2 rRNS és 16-féle tRNS esetében a DNS nehézszála, a többinél a könnyűszál képezi a kódoló szálat. Tehát összesen 37 gén van az mtDNS-ben, amelyek szinte hézagmentesen kapcsolódnak egymáshoz. Ezekben nincsenek köztesek, csak képezőkből tevődnek össze. Egyetlen nem kódoló rész egy rövid D-hurok (D-loop). Az mtDNS genetikai kódja 4 kodonban eltér a sejtmagi DNS kódjától, ezért az itt található gének csak az energiatermecsben fejeződhetnek ki.
Az mtDNS-ek száma egy energiatermecsben 2–10, az egész sejtben több száz, akár ezer is lehet. Ugyancsak különböznek abban, hogy az energiatermecsi DNS kettőződése független a sejtkörtől, és végbemegy a teljesen kiérett, nem osztódó sejtekben (pl. idegsejt, izomsejt) is. Az mtDNS anyai ágon öröklődik, egy-egy kivétel azonban előfordul.
Az energiatermecsi RNS-ekben az elektronleadási folyamatok miatt gyakoriak a másulások, amelyek betegségeket okozhatnak. Több mint százféle olyan pontmásulásuk ismert, amely betegséghez vezet. A pontmásulások többsége a tRNS-ekben fordul elő; súlyos betegségeket idézhetnek elő, mint például a MELAS (mitochondrial encephalomyopathy, lactic acidosis and stroke-like episodes), amely agyvelőbántalommal, tejsavasodással és szélütés-szerű tünetekkel jár, és leggyakrabban az m.3243A>G másulás okozza. Az mRNS-eket kódoló génekben negyvennél több betegséget okozó pontmásulás ismert, például az m.3460G>A másulás, amely a Leber-féle örökletes optikus neuropátiát (LHON) váltja ki, vagy a MERRF tünetcsoport (Myoclonic Epilepsy with Ragged-Red Fibers syndrome), amely az m.8344A>G másulásból keletkezik. Pontmásulások a rRNS-eket kódoló génekben is ismertek, pl. az m.1555A>G, vagy az m.1494C>T. Ezek összefüggnek az időskori hallásvesztéssel, és kapcsolatuk van az autizmussal is. Leírtak energiatermecsi DNS-vesztést, sőt hiányt is. A másulások által keletkezett betegségeket energiatermecsi betegségeknek nevezzük.
genomtan, genomika (DNS-tan) genomics a genomot (a bázispárok összességét) elemző tudomány.
genomikai genomic a genommal (DNS-sel) kapcsolatos, arra vonatkozó.
genomikus a genomikával (DNS-sel) foglalkozó személy.
rákgenomtan (onkogenomtan) cancer genomics, oncogenomics a ráksejtek (daganatsejtek) DNS-szerkezeteit (bázisait és azok működését) vizsgáló tudomány.
hisztonkötött DNS dyad position a hisztonmag körüli DNS; ellentétben van a magtestecskék közötti összekötő DNS-sel.
keringő daganat-DNS (ctDNS) circulating tumor DNA, ctDNA a daganatból vagy a keringő daganatsejtekből származó piciny (~120–180 bázispárnyi [1 magtestecs és az összekötő szál]) DNS-darab a vérplazmában vagy más testnedvben. Származhat az elhaló vagy sejtvégzeti daganatsejtekből, de elválaszthatja az élő daganatsejt is. Nem tévesztendő össze a szérumban szabadon keringő DNS-sel (cell-free DNA, cfDNA). Miután a daganatból származik, tükrözi a daganatsejt DNS-ét, ezért használják génhiba kimutatására is, pl. szokványos a végbél-vastagbél daganatokban a RAS gén vizsgálatára. Alkalmazható továbbá a kezelésre adott válasz megítélésére, valamint a rejtett maradékbetegség (a kiújulás) jelzésére, pl. a kezelést 2–4 héttel követően jelen lévő ctDNS maradékbetegségre utal; ebből újul ki a daganat. A kiújuló daganatból származó ctDNS szerkezete általában más (más génhiba), mint az elsődleges daganatból származóké, utalva a kiújuló daganat fejlődésére. Lévén, hogy a kiújuló daganatból származik, molekulakezelési célpont is lehet, pl. a PD1-gátlók akadályozhatják a kiújuló daganat fejlődését. A ctDNS-t szokásosan a vérből, ritkábban más testnedvből nyerjük ki (liquid biopsy), azonosításához sajátos genetikai vizsgálatokat alkalmaznak. A vérből vett mintának két nagy hátránya van: 1. kevés a ctDNS, 2. keveredik a nem daganatsejtes eredetű keringő DNS-sel (cfDNS, cell-free DNA).
köpenyes DNS* nucleocapsid (nukleokapszid) a vírus DNS-e a fehérjeköpenyével együtt. Ez a
vírusmag, önmagában egyik sem lehetséges.
POLε (DNS-polimeráz-ε) DNA polimerase epsilon (a nemzetközi irodalomban többnyire POLE formájában írják) az egyik legjelentősebb DNS-t másoló enzim: POLδ és a POLα fehérjékkel együtt másolja a DNS-t. A POLε a DNS vezetőszálának másolásáért felelős, a másik kettő a késlekedőszálat teszi hozzá. A POLε nagy sarkalló egységből (catalytic p261 subunit), kisebb nem sarkalló (noncatalytic p59) és két kis (p17 és p12) egységből tevődik össze. A sarkalló egység tartalmazza az átirat-ellenőrző gomolyt* (proofreading exonuclease domain); ez másolja a DNS-t, és kijavítja a DNS 3’- és 5’-végi hibáját, pl. a másolódáskor hibásan beiktatódott nukleotidot kivágja. Részt vesz továbbá az egy- és kétszálú DNS-törések kijavításában. A többi egység közreműködik a DNS-kettőződés és a DNS-hibajavítás folyamataiban. A POLε fehérje sarkalló egységét a POLE gén kódolja; ez gén a 12-es kromoszómán van (12q24.33). A POLε fehérje többi részének képzésében POLE2, POLE3 és a POLE4 gén is részt vesz.
végrész-DNS (→végrész)
zDNS (→DNS kettős csavarodás)
Találatok alcímszavakban (2 szócikk):
DNáz (dezoxiribonukleáz) deoxyribonuclease, DNase a DNS foszfodiészter kötését vízzel bontó enzim. Sokféle ismert, családokat alkotnak. Támadáspontjuk szerint megkülönböztetjük az endo- és exodezoxiribonukleázokat (endoDNáz, DNS-endonukleáz; exoDNáz, DNS-exonukleáz).
DNS-endonukleáz endoDNáz, DNA endonuclease a DNS-gerinc belső foszfodiészter kötéseit bontja; hosszabb-rövidebb nukleotidcsoportok jönnek létre. Két nagy vegyes osztályuk a DNáz1 és DNáz2 (DNase I, DNase II). Jelentősek a sejtvégzetben és betegségek kialakulásában. (→APE1) Sajátos a végendonukleáz (flap endonuclease), amely szabadon áll (nem kapcsolódik hidrogénkötéssel a kiegészítő DNS-hez), és a DNS-végről távolít el nukleotidokat.
DNS-exonukleáz DNA exonuclease a nukleinsavak végéről hasít le egyes nukleotidokat; a végeken bontja a foszfodiészter-kötést. (→nukleáz).
RNS-polimeráz RNA polymerase, RNAP (POL) az RNS-t képző enzim. Két alapformája a DNS-függő és az RNS-függő RNS-polimeráz. Az előbbi a DNS-t, az utóbbi az RNS-t használja mintafelületnek.
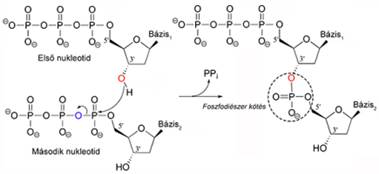 DNS-függő RNS-polimeráz DNA dependent/directed RNA polymerase, DdRP DNS-ről RNS-t képző enzim; egyszálú DNS-t másol, az
átírt nukleotidokat köti össze foszfodiészter-kötéssel. Képes összekapcsolni az
első nukleotidot a másodikkal, miként a továbbiakat is; tevékenységéhez tehát
nem szükséges indítószál (primer).
DNS-függő RNS-polimeráz DNA dependent/directed RNA polymerase, DdRP DNS-ről RNS-t képző enzim; egyszálú DNS-t másol, az
átírt nukleotidokat köti össze foszfodiészter-kötéssel. Képes összekapcsolni az
első nukleotidot a másodikkal, miként a továbbiakat is; tevékenységéhez tehát
nem szükséges indítószál (primer).
A másolódott nukleotid 5’-végén trifoszfát, 3’-végén OH-csoport van. A polimeráz ezeket kapcsolja össze. Az ábra az elsőként és másodikként másolódott nukleotidot mutatja. A második trifoszfátjából két foszfor (pirofoszfát) hasad le; így jön létre a kötés. Az elsőn megmarad a trifoszfát.
A DNS-hez az átírásfehérjék toborozzák a polimerázt; önmagában nem képes a bázissorok megkülönböztetésére. Nincs nukleáz működése, ezért az RNS-képződés esetleges hibáit nem javítja ki. Ennek azonban nincs nagy jelentősége, mert általában egyszerre nagyon sok szabályos RNS is képződik, és így egy-két hibás RNS hatása gyakorlatilag nem jut kifejezésre. Ám, ha sok a hibás RNS, sejtműködési zavar keletkezik.
A DNS-függő RNS-polimerázoknak többegységes és egyegységes formája is van; szokványosan az előbbieket nevezzük egyszerűen RNS-polimerázoknak. Az emberi sejtekben az egyegységes forma az energiatestecsekben, a többegységes a sejtmagban fordul elő. Az utóbbinak három formája ismert, az RNS-polimeráz-I, -II, -III. Ezek laboratóriumi megkülönböztetésére a gyilkos galóca mérgét (α-amanitin) használják: a méreg az RNS-polimeráz-II-t megbénítja, az RNS-polimeráz-III-at csak részben gátolja, az RNS-polimeráz-I-et pedig egyáltalán nem. Az mRNS-t csak az RNS-polimeráz-II írja át.
Egyegységes RNS-polimeráz single-subunit RNA polymerase (Egyéb nevek: ssDdRP, POLRMT, T7 RNS-polimeráz) a baktériumokat támadó bizonyos vírusok (phage 7) jellegzetes polimeráza, az emberi sejtekben az energiatestecsekben van jelen. Az energiatestecsi DNS-t írja át járulékos átírásfehérjék (TFAM, TFB2M) segítségével. Főleg az energiaigényes szövetekben (szív, agy, vese) van jelentősége: ezekben az RNS-ek 10–30%-át ezek adják. Átírási hiba zavart kelthet az energiatestecsek működésében.
Többegységes RNS-polimerázok multiple-subunit RNA polymerases
▪ RNS-polimeráz-I (RNA polímerase I, RNAP I) a sejtmagvacskában található, a 47S elő-rRNS-t képezi, amely 18S, 5,8S és a 28S rRNS-ekké alakul. Ezek és a polimeráz-III által másolt 5S RNS alkotja a ribotestecs RNS összetevőjét. A polimeáz-I kizárólag az rRNS-gének (multicopy rRNA genes) átírására képes enzim, és az átírások ~70%-át végzi. Szabálytalan működése rák és rRNS-ártalmak kialakulásához vezet. A rákelleni kezelés egyik célfehérjéje is lehet.
▪ RNS-polimeráz-II (RNA polimeráz II, RNAP II) az elő-mRNS-t átíró enzim, de másol kis magi RNS-eket is (pl. piRNS). Az emberi polimeráz-II 12 törzsökös alegységből (RPB1–12) álló, 550 kDa tömegű fehérje. A sarkalló törzsegysége mellett a legnagyobb alegysége a CTD gomolyt (carboxi terminal domain) tartalmazó RBP1, amely a C-végen lévő enzim. A POLR2A gén kódolja. Ez kapcsolja össze az RNS átíródásának és érésének folyamatát, fontos szerepe van az átírás indításában is. Jellegzetes a hetes (Tyr1, Ser2, Pro3, Thr4, Ser5, Pro6, Ser7) ismétletekből álló mintázata; ez érzékeli a jelzéseket, és elősegíti a fehérjék kötődését a hisztonok módosítására. Csak az átírásfehérjét kötött indítóhoz kétes kapcsolódni. (→indító)
▪ RNS-polimeráz-III a szállító RNS (tRNS) és a kis sejtmagi RNS-ek (snRNS) többségét képezi, elemi tartozéka az RNS-szikének.
RNS-függő RNS-polimeráz RNA dependent/directed RNA polymerase, RdRP, RNA-replicase RNS-t RNS-ről, nem DNS-ről átíró enzim. RNS-mintafelületről készíti annak kiegészítő másolatát. Így sokszorozódnak az RNS-vírusok, de előfordul magsejtűekben is (cellular RdRP, cRdRP).
Részleges egyezések (13 szócikk):
circulating tumor DNA (ctDNA) →keringő daganat-DNS
ctDNA (circulating tumor DNA) →keringő daganat-DNS
DNA damage response (DDR) →DNS-károsodási válasz
DNA recombination →DNS-átrendeződés
dyad position →hisztonkötött DNS
energiatermecsi DNS-osztódás mitochondrial DNA replication (mitokondrium-DNS) A folyamat másolja a sejtkört, annak része, és a szabályozása is
egyezik. A DNS-kettőződést a DNS-polomeráz-γ enzimegyüttes végzi. Ez egy 140
kDa tömegű, sarkalló DNS-polimerázból, a POLG gén kódolja, és két 55 kDA
járulékos alegységből áll, ezeket a POLG2 gén kódolja. A kettőződési testecs,
amelybe a DNS-polimeráz, egy helikáz (TWINKLE) és az energiatestecsi SSB
fehérjékből áll.
fehérjeköpenyes vírus DNS/RNS nucleocapszid a vírus DNS vagy RNS és fehérjeköpenyének együttes neve.
ismétlet* repeat, DNA repeat, repeated sequence, repetitive element, repeating unit, satellite olyan bázissorok, amelyek többszörösen ismétlődnek a DNS-ben. Elhelyezkedésük alapján vannak egymással érintkezők (tandem repeats) és olyanok, amelyek a DNS különböző részein jelennek meg; ezek a szétszórt ismétletek (interspersed repeats). Jellemzőjük, hogy képesek a DNS egyik helyéről áttevődni másik, ezért szóródtak szét. Voltaképpen ugrálatok (transposons) (→ugrálat). Meghatározás szerint nem tartoznak az ismétlet fogalmába.
Az ismétletek mind a két DNS szálon vannak. Az egyik szálon lévő ismétlet a másikon a kiegészítő bázisok szerint jelenik meg. Azok is ismétletek, csak a kiegészítő bázisok szerintiek. Tehát például, ha érintkező ismétlet van az 1-es kromoszóma egyik DNS-szálán, akkor ugyanazon helyen lévő másik DNS-szálon is érintkező ismétlet van, természetesen a kiegészítő bázisoknak megfelelően.
Az ismétletek válzatában elvben azonos ismétletek vannak. Például az 1-es kromoszóma (mondjuk apai) egy helyén ismétlek vannak, a másik 1-es kromoszóma (anyai) ugyanazon helyén is azonos ismétleteket látunk. Ám ez nincs mindig így, mert az ismétletek nagyon változékonyak, és lehet, hogy a szülők adott vázlataiban eltérnek. A legnagyobb eltérés az érintkező ismétletek számában fordul elő, más az anyaiban, más az apaiban. Ez lehetővé teszi, hogy az ismétletek számának vizsgálatával nyomon követhessük a válzatokat az öröklődésben nemzedékről nemzedékre. Ezt a módszert nevezzük válzatkövetésnek (allele tracking).
Megjegyzések:
▪ A satellite elnevezés a DNS régi (cézium-szulfát töménységén alapuló) centrifugálási vizsgálatából (cesium density gradient ultracentrifugation) származik: a csőben a meghatározó DNS-tömeg elkülönül a vékony kísérő (satellite) rétegtől, amely az ismétleteket tartalmazza. Ezeket az ismétleteket HSat1–3-nak (human satellite 1-3) nevezték el.
▪ HSat1A 42 bp nagyságú, AT-ben gazdag ismétlet a 3-as, a 4-es és a 13-as kromoszómán.
▪ HSat1B 2420 bp nagyságú ismétlet az Y-kromoszómán.
▪ HSat2 (CATTCGATTC )n származékok az 1-es és a 16-os kromoszómán.
▪ HSat3 (CATTC)n származékok a 9-es, a 13–15-ös a 21–22-es és az Y-kromoszómán.
A HSat1–3-mat a nemzetközi irodalomban classical human satellite-nak nevezik. A közbenesköri kromatin DNS-e: óriás (átlagosan 100 megabázis) ismétletsorok – a DNS-nek ~3%-át teszik ki.
Előfordul a nemzetközi meghatározásokban az alphha satillite DNA (αSat), amelyik a kromoszómák közbenesének óriás ismétleteit jelöli. (→közbenes)
A hazai szóhasználatban ne mondunk szatellita DNS-t;
pontosítsuk, hogy milyen ismétletről van szó, például mikroismétlet.
■ Az ismétlet bázisainak száma szerint megkülönböztetünk:
▪ Mikroismétleteket* (microsatellites, más néven: short tandem repeats, STRs vagy simple sequence repeats, SSRs): egy-egy ismétletben 1–6 bázis van. (→mikroismétletek)
▪ Kis ismétleteket* (minisatellites): egy ismétlet 10–100 bázisból áll; szokásosan 30–35 bázispár, 10–15 bázisnyi törzsrésszel. Az ismétletek száma egy-egy ismétletsorban igen változó (1–15 kB), ezért nevezik számváltó ismétleteknek* is.
▪ Óriás ismétleteket* (macrosatellites), amelyeknek egy ismétletében >100 bázis van, rendszerint néhány száz. Ezek ismétlődve kiterjedhetnek megabázis nagyságúra, ezért nevezzük óriás ismétletnek. Két formája a HSat1–3 és az αSat.
■ Az ismétletek egymáshoz viszonyított jellege az ismétletmintázat, amely többféle lehet:
▪ Egyenes ismétletek* (direct repeats): a mintázatok egy irányban vannak. Lehetnek egymástól elválasztva, például TATCGGnnnnTATCGG, vagy érintkezők, amelyeket fej–láb ismétleteknek (head-to-tail tandem repeats) nevezünk: az egyik ismétlet vége kapcsolódik a következő elejéhez. Például CAGCAGCAGCAG… (a bázishármas-mintázat vége kapcsolódik a következő bázishármas elejéhez). Az emberi DNS több mint egymillió fej–láb ismétletet tartalmaz; ezek a genetikai állomány ~3 százalékát teszik ki.
▪ Ellentett ismétletek* (inverted repeats): olyan ismétletek, amelyek az egyik DNS-szálon 5’–3’ irányban olvasva azonosak a másik (kiegészítő) DNS-szálon 5’–3’ irányban olvasható bázissorokkal. Például TTACGCGTAA – a CGTAA a kiegészítő DNS-szálon 5’–3’ irányban olvasva: TTAGC. Lehetnek egymástól elválasztva is: TTACGnnnCGTAA. Sajátos formája a visszafutó ismétlet (palindromic repeat), amely olyan ellentett ismétlet, amelynek a betűsora elölről és hátulról olvasva is ugyanaz. Jellegzetes példa az ösztrogénjelfogót kötő ösztrogén-válaszelem ismétlete: AGGTCAnnnTGACCT. A TGACCT a kiegészítő szálon 5’ – 3’ irányban olvasva: ACTGGA. Vagyis, az AGGTCA ismétlet betűsora visszafelé olvasva (ACTGGA) egyezik azzal a betűsorral, amelyet a kiegészítő DNS-szálon olvasok 5’–3’ irányban.
Az ismétletek a Mendel-szabályok szerint öröklődnek, rendkívül változatosak, jellemzők az egyedre. A DNS ismétleteket tartalmazó részei kevéssé állékonyak; hajlamosok másulásra, példál a DNS kettőződésekor, és bővülésre. Az ismétletek bővülése (számuknak növekedése) összefügghet betegségek, leginkább idegrendszeri betegségek kialakulásával, például a mikroismétletek bővülése negyvennél több idegrendszeri betegség okozója.
köpenyes DNS/RNS nucleocapsid (nukleokapszid) a vírus DNS/RNS és köpenyének együttes neve.
(→vírusszerkezet)
nucleocapsid (nukleokapszid) →köpenyes DNS/RNS
replication (replikáció) →DNS-kettőződés
restriction enzyme →DNS-hasító enzim
topoizomeráz →DNS-topoizomeráz