állapotegyensúly system equilibrium a rendszert alkotó részecskék egyenletes eloszlása. Az állapotjellemzők egyike sem változik. (→állapotjellemző, rendszer)
Részleges egyezések (46 szócikk):
BCR fehérje breakpoint cluster region protein, BCR, más néven: renal carcinoma antigen NY-REN-26szerin-tirozin-kináz; a BCR gén kódolja. A BCR gén a 9-es kromoszóma hosszú karján van (9q34); egyike a BCR-ABL1 felemás génnek, amely a Philadrlphia-kromoszómán van. Tevékenysége részben ismert; a GTPázokrho-családjának (rhoA) guanin-nukleotid cserélő tényezője.
beágyazódott gén* nested gene (→gén)
CD ( clusters of differentiation) a sejtfelszíni fehérjék CD-antigének szerinti osztályozásának nemzetközi rendszere. A CD-antigéneket fajlagos ellenanyagokkal határozzák meg.
CD28 ( clusters of differentiation 28) sejtfelszíni jelfogócsalád, hasonló szerkezetű sejtfelszíni fehérjék. Három gomolyuk (sejtkívüli, sejthártyai, sejtbeli) van. Jellemző az immunglobulinszerű változó sejtkívüli gomoly sajátos mintázata; a sejtbeli gomolyban tirozin van. A CD28 a fehérjecsalád alapító tagja. Egyéb tagjai: ICOS, CTLA4, PD1, PD1H, TIGIT, and BTLA. A B7 fehérjékkel kapcsolódnak.
CD28 fehérje a T-sejtek felszínén lévő jelfogó; a CD4 T-sejtek ~80, a CD8 T-sejtek ~50%-án van jelen állandóan. A kifejeződése a korral csökken. Az alapszintű folyamatos jelenlétük teszi lehetővé a Treg-sejtek állandó működését, az autoimmunitás kivédését.
A CD28 az éretlen T-sejtek legfontosabb érője. Az érett T-sejteken meghatározó az IL2 és más citokinek, továbbá kemokinek képzésében és a T-sejt megmaradásában (túlélésjelek, BCLxL). Befolyásolja a T-sejt anyagcseréjét, sajátosan foszforilez, serkenti számos gén átírását, és módosítja az aktinsejtvázat is. Végeredményben hatása rendkívül szerteágazó.
A B71/2-vel kötődik a pMHC–TCR társulás hatására, de kapcsolódik a B7H2-vel is. A sejtplazmai mintázataihoz sokféle fehérje kapcsolódhat (SHIP1, SLP76, GRAP, CBL, ITK, PI3K, GRB2, GADS, CSK, STS1, PTPN11, VAV3, CIN85, LCK, FLNA, CD2AP), lehetővé téve számos jelközvetítést.
A CD28 megjelenik a csontvelősejteken, a neutrofil és az eozinofil fehérvérsejteken, valamint a plazmasejteken, elősegítve az ellenanyag képződését.
CTLA4 (cytotoxic T-lymphocyte-antigen 4) fehérje (egyéb elnevezései: cytotoxic T-lymphocyte-associated protein 4, CD152 fehérje) jelfogógátló fehérje a T-, B-, NK, NKT, DC sejtekben. Immunellenőrző pontként viselkedik: gátolja a sejtosztódást és az IL2 képződését, továbbá befolyásolja az eredeti CD4+-T-sejtek elkülönülését, de szabályozza a T-sejtek végrehajtó tevékenységét is, pl. a B-sejtekre gyakorolt hatást.
Ha a CTLA4 gátolt/hibás, felszaporodnak a TH2-sejtek, kivált a TH17-sejtek. A CTLA4 a szabályozó T-sejteken (Treg) állandóan jelen van, egyéb T-sejtekben a mag körüli Golgi-hálózatban, a beltestecsben és az emésztőtestecsekben található; folyamatosan áramlik a sejtfelszínre, de csak foszforilezett állapotban marad ott. Az antigénbemutató sejtek B71/2 és a B7H2 fehérjéjével kötődik.
A CTLA4 gén (2q33.2) négyféle CTLA4-et kódol, és gyakori a sokalakúság is; ezek különböző módon hatnak, és különböző, elsősorban autoimmun betegségekkel függnek össze.
PD1 ( programmed death-1) fehérje (egyéb neve: PDCD1) gátló jelfogó a CD4- és a CD8-T-sejtekben, az NK, NKT és B-sejtekben, a nagyfalókban és néhány DC-sejtben. A T-sejtekben gátolja a jelközvetítéseket (PI3K, RAS–MAK), a citokinek és a végrehajtó működéséhez szükséges átírásfehérjék képződését, csökkenti a T-sejtek mozgását, kapcsolódását más sejtekkel és a sejtpusztító hatását; a sejtvégzeti molekulák felszaporodásához vezet.
A PD1 jelzés hatására jelenik meg a sejt felszínén tevősítéskor vagy idült gyulladásnál; egyébként a sejtplazmában van. A T-sejteken a pMHC–TRC kapcsolódás, továbbá IL2, IL7, IL15, IL21 és I-es formájú IFN hatására fejeződik ki. Sejtfelszíni megjelenését még a sejt anyagcseréje is befolyásolja: glükozbontáskor csökken, ösztrogén hatására viszont fokozódik. Átmenetileg az eredeti T-sejtek felszínén is jelen van.
Ha a serkentés folyamatos (idült gyulladás), a PD1 folyvást kerül a sejt felszínére, aminek következtében a T-sejt működése zavarttá válik – ezt nevezzük T-sejt-kimerülésnek (T cell exhaustion).
A PD1 a PDL1 (programmed death-1 ligand) és a PDL2 (programmed death-2 ligand) jelvivőkkel kapcsolódik.
A PD1 gén (2q37.3) négyféle PD1-t képes kódolni, köztük vízoldékony változatot. Gyakori a sokalakúság is. Ezek is különbözök, és összefüggnek autoimmun betegségekkel. (→PD1)
ICOS ( inducible costimulator) serkentő T-sejt felszíni jelfogó; a TCR kapcsolódására fejeződik ki. Főleg a Th2-, kevésbé a Th1-sejteket serkenti, elősegíti az IL10 képződését a szabályozó T-sejtek fenntartásához.
CD40 ( clusters of differentiation 40) a TNF-családba tartozik. A B-sejtek, a nagyfalók és a tüszői nyúlványos sejtek (FDC) felszínén kifejeződő fehérje; összekötődik a T-sejtek CD40L-jével. A kapcsolódás folytán az fenti antigén-bemutató sejtek képeznek IL12-t, ez pedig fokozza a CD4Th1m a CD8, az NK-sejtek és a B-sejtek működését, továbbá a B-sejtek átalakulását plazmasejtekké, illetőleg emlékező B-sejtekké.
cohort cluster →csoport
 csecsemőmirigy (kedezmirigy) thymus a szegycsont mögött, a mellüreg felső
részében (mediastinum supracardiacum) elhelyezkedő, kötőszöveti tokba zárt,
lebenyes nyirokszerv; nevezik lymphoepithelialis nyirokszervnek is. Születéskor
jelentős nagyságú (~30 g), a serdülésig növekszik, de a serdülés alatt,
hormonok hatására, javarészt visszafejlődik, és zsírszövet foglalja el a
helyét; megmaradnak azonban működő kisebb szigetek.
csecsemőmirigy (kedezmirigy) thymus a szegycsont mögött, a mellüreg felső
részében (mediastinum supracardiacum) elhelyezkedő, kötőszöveti tokba zárt,
lebenyes nyirokszerv; nevezik lymphoepithelialis nyirokszervnek is. Születéskor
jelentős nagyságú (~30 g), a serdülésig növekszik, de a serdülés alatt,
hormonok hatására, javarészt visszafejlődik, és zsírszövet foglalja el a
helyét; megmaradnak azonban működő kisebb szigetek.
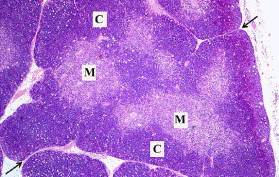
Két nagyobb lebenyét kötőszövetei sövények tagolják lebenykékre. A sövényekben erek és az elvezető nyirokér fut – odavezető nyirokér nincs. A mindegyik lebenyke külső kérgi és belső velőrészből áll. A tokból jövő kötőszöveti sövények tagolják a lebenykék kérgi részét is, de a velőállományt már nem; csupán az ereket szállítják a velőállományhoz. Helyenként magas érhámú visszerecske is előfordul.
Az ábrán látható, hogy a tokból kiinduló sövények (nyilak) lebenykékre tagolják a csecsemőmirigy jobb és bal oldali lebenyét. Csak a kéreg (C) tagolódik, a velőállomány (M) egységes. A sövények vége a velőállományhoz kapcsolódik, bennük erek futnak. A kép egy lebenykét ábrázol. (Oláh Imre felvétele)
A csecsemőmirigy alapvázának (stroma) felépítése sajátos: megnyúlt hámsejtek térhálózata alkotja rostok nélkül, vagyis nem mesenchimalis eredetű hálózatsejtekből épül fel (nem térrács), hanem endo- és ectodermalis származású, desmosomákkal kapcsolódó, különleges hámsejtekből (hámrács) (l. feljebb). Ezek a hámsejtek termelnek TSLP-t (thymic stromal lymphoprotein; nyúlványos sejteket serkentő hormon). A hámrácssejteknek több formája is van:
• A kérgi részben a hámsejtek nyúlványaikkal körbefogják a T-nyiroksejteket – egy-egy hámsejt több százat is –, bemutatják az MHC1 és az MHC2-molekuláikat a nyiroksejteknek, és IL7-et képeznek, ezzel elősegítik a T sejtek kiválogatódását és érését. Ezek a nagy kérgi hámsejtek (cortical thymic epithelial cell [cTEC]) dajkasejtek (nurse cells).
• A hámsejtek a velőállományban (medulary thymic epithelial cell [mTEC]) vaskosabbak, felszínükön, a nyiroksejtek negatív kiválasztódásában fontos fehérjék (PTH, trioglobulin, CRP, inzulin stb.) vannak.

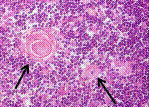 A csecsemőmirigy T-nyiroksejtjei a thymocyták. A
hámrács közeiben tömegestől vannak, keverednek a nagyfalósejtekkel és a
nyúlványos sejtekkel; az utóbbiak főleg a velőállományban fordulnak elő.
A csecsemőmirigy T-nyiroksejtjei a thymocyták. A
hámrács közeiben tömegestől vannak, keverednek a nagyfalósejtekkel és a
nyúlványos sejtekkel; az utóbbiak főleg a velőállományban fordulnak elő.
Hassall-testek Hassall’s corpuscles a csecsemőmirigy jellegzetes képződményei a velőállományban. Ezek körkörös hámsejtrétegekből felépülő, közepükön keratinizálódott képletek. Az elszarusodott hámsejtek hagymalevélszerűen rendeződnek. Az ábrákon a Hassall-testeket nyilak jelölik. A nagyítás a Hassal-test elektronmikroszkópos képe. (Oláh Imre felvétele.)
diastereomers (diasztereomerek) →nem tükörképi azonmások
ébrényi őssejtek embryonic stem cells a korai ébrénycsomó sejtjeit, illetve az ébrénycsomó későbbi felsőbb sejtjeit (epiblast) nevezzük ébrényi őssejteknek.
elektromos tér electric field, E-tér a fizikában az a közeg, amely a töltések egymásra hatását közvetíti. Minden elektromos töltés elektromos teret hoz létre maga körül; ez a töltéssel bíró anyag tulajdonsága. Az elektromos tér a töltéstől távolodva a távolság négyzetével fordított arányban csökken. Elektromos tér azonban a változó mágneses tér hatására is keletkezik. A nyugalmi (static) elektromos töltés által létrehozott elektromos tér a nyugalmi elektromos tér* (static electric field).
Az elektromos teret az elektromos erővonalakkal* (electric lines) jelöljük:
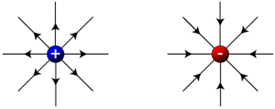
A pozitív töltés körüli elektromos vonalak távolodnak a töltéstől, a negatív töltésnél a töltés felé haladnak.
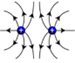
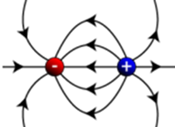 Elektron és proton között kétsarkú elektromos tér* (dipole
electric field) van. A töltések egyforma nagyságúak, a köztük lévő távolság
kicsi. A tér iránytér: a negatív töltéstől a pozitív töltés felé mutat. Az
elektromos vonalak (egyezményesen) a pozitívtól a negatív felé haladnak, abban
végződnek. Tehát nincs olyan, amelyik a semmiben végződik, és olyan sem, amelyik
önmagába tér vissza, vagyis zárt erővonal. Az erővonalak soha nem metszik
egymást, ugyanis ha metszenék egymást, két irányba kellene haladniuk, ez pedig
lehetetlen. Úgy mondjuk, hogy a kétsarkú elektromos tér „örvénymentes”
iránymező. Ez azonban nem jelenti azt, hogy a pontszerű elektromos töltéseknek
az erővonalak mentén kellene haladniuk.
Elektron és proton között kétsarkú elektromos tér* (dipole
electric field) van. A töltések egyforma nagyságúak, a köztük lévő távolság
kicsi. A tér iránytér: a negatív töltéstől a pozitív töltés felé mutat. Az
elektromos vonalak (egyezményesen) a pozitívtól a negatív felé haladnak, abban
végződnek. Tehát nincs olyan, amelyik a semmiben végződik, és olyan sem, amelyik
önmagába tér vissza, vagyis zárt erővonal. Az erővonalak soha nem metszik
egymást, ugyanis ha metszenék egymást, két irányba kellene haladniuk, ez pedig
lehetetlen. Úgy mondjuk, hogy a kétsarkú elektromos tér „örvénymentes”
iránymező. Ez azonban nem jelenti azt, hogy a pontszerű elektromos töltéseknek
az erővonalak mentén kellene haladniuk.
Azonos töltéseknél a mezők nem hatnak egymásra.
Az elektromos tér (E) ereje a tér valamelyik pontján egyenlő az adott ponton lévő megfigyelési töltésre ható elektromos erő és töltés hányadosával: E = Fe / q (E kifelé terjedő elektromos mező, F elektromos erő, q az elektromos teret létrehozó részecske töltése). Az elektromos erőt newtonban, a töltést coulomb-ban fejezzük ki, így az elektromos térerősség mértékegysége = newton/coulomb (N/C = V/m). A képletből adódik, hogy a töltésre ható elektromos erő a töltés és az elektromos térerősség szorzata.
kétsarkú elektromos testek (dipolusok) azok a testek, amelyekben a pozitív
és a negatív elektromos vég elkülönül; az ellentétes töltések középpontja a
rendszeren belül nem egy pontban van. Ezeknek a testeknek kétsarkú elektromos
terük van. Az elektromos térbe helyezett kétsarkú elektromos testekre
forgatóerő hat, amely a testet a tér irányába igyekszik fordítani. A forgatóerő
nagysága arányos a kétsarkú nyomatékkal.
A molekulák is lehetnek kétsarkúak.
kétsarkú nyomaték dipole moment (dipolusmomentum, dipolusnyomaték)
a kétsarkú elektromos testek egyik sajátsága: az elektromos térbe helyezett
kétsarkú elektromos testek ellenállása a tér forgatóhatásával szemben. Jele: p;
mértéke: q × l (a q a töltés, az l a +q és a -q töltések közötti
távolság). Mértékegysége: coulomb × méter, C × m.
embryonic stem cells (→ébrényi őssejtek)
enzimnevek az enzimek nemzetközi elnevezései. Ezek angol nevek, amelyeket a Biokémiai és Molekolabiológiai Nemzetközi Szövetség Enzim Bizottsága (International Union of Biochemistry and Molecular Biology, Enzyme Commission, EC) határoz meg, és tesz naprakésszé időről időre. Mindegyik enzimnek van rendszerneve és besorolási száma (EC-szám). Számos enzimnek van közkeletű neve is (arbitrary name). Az enzimek nemzetközi jegyzékében az enzimek neve az EC-számokkal kezdődik, ezt követi a közkeletű név zárójelben, ha van, majd a rendszernév.
rendszernév systematic name a nemzetközi névben -ase végződésű, amelyet a vegylet nevéhez (tyrosinase), vagy az enzim által előmozdított vegyfolyamat nevéhez (dehydrogenase, decarboxylase) illesztenek. A magyar rendszernevet magyarosan írjuk -áz végződéssel (tirozináz, dehidrogenáz).
Az -áz (-ase) végződése kizárólag egyedi enzimeknek lehet, más molekuláknak és az enzimrendszereknek (két- vagy többenzimes folyamatok) nem. Az utóbbi esetben az enzim neve után kiírjuk, hogy rendszer (system) (piruvát-dehidrogenáz-rendszer; pyruvate dehydrogenase system).
közkeletű név arbitrary/trivial name az egyedi enzimre utal, például pepsin, tripsin. Nem ritkán a rendszernév mozaikszója (SCAD [short chain acyl-CoA-dehydrogenase]). Nem hivatalos névként jelölhetjük az enzimeket valamilyen tulajdonságuk/összetevőjük és az enzim szó társításával (flavin, biotin, piridoxál-foszfát enzimek).
EC-szám (EC – Enzyme Commission) az enzim azonosítására szolgál, megjelöli az enzim helyét az enzimek osztályrendszerében. Négyjegyű, ponttal elválasztott arab szám. Az első szám jelöli az osztályt, a második az alosztályt, a harmadik a csoportot, a negyedik pedig az egyedi enzimet, például 2.1.1.2. (az enzimek második osztálya első alosztályának első csoportjába tartozó második enzim). Az EC-számot nevezhetjük számjelnévnek is. Írása: EC 2.1.1.2. az első száma a transzferáz, a második a hatáscsoport (carboxil [EC 2.1.], keton/aldahid [EC 2.2.], acetil [EC 2.3.] stb., a harmadik a hatáscsoport további részletezése (metiltranszferáz [EC 2.1.1.], hydroximetiltransferáz [EC 2.1.2.] stb., a negyedik az egyedi enzim (metiltranszferáz-2).
forgás rotation a hagyományos fizikában valamely test tengelye vagy középpontja körüli mozgása, a forgatónyomaték hatására jön létre. A test minden pontja a forgástengely (középpont) körül mozog. A forgás nem egyenes irányú, hanem a tengellyel szöget (ω) bezáró mozgás.
Háromféle fizikai forgást különböztethetünk meg:
▪ A tengely körüli forgás a testnek a rögzített tengelye körüli körbeforgása; a test minden pontja a tengelye (forgástengely) körüli körpályán mozog. A forgástengely irányát a jobb kéz hüvelykujja mutatja, ha az ujjakat a forgás irányába állítjuk, a hüvelykujjat 90°-ban kinyújtjuk a kézfej többi részéhez képest. A tengely irányát nyíllal jelöljük, a nyíl annál hosszabb, minél gyorsabb a forgás.
▪ A pontszerű forgás a középponthoz (forgáspont) rögzített test körbeforgása. Például a középponthoz zsinórral erősített labda körforgása. Ez is tengely körüli forgás, csak a tengely időben változik
▪ A pörgettyű a test egy pontján rögzített forgómozgás.
A forgásirányt a jobb kéz szabállyal állapíthatjuk meg: ha ujjainkat a forgás irányába hajlítjuk, a hüvelykujj mutatja az irányt.
forgásmennyiség (perdület) a forgó test forgásának mennyisége, a test forgásállapotát jellemző iránymennyiség. A tehetetlenségi nyomaték és a szögsebesség szorzata. Jele: N, mértéke: θ × ω. Mértékegysége: kg × m2 × 1/s.
Zárt tér összes perdülete állandó, azaz a perdület csak külső erő hatására változik meg. Ez a perdület megmaradásának törvénye.
forgássebesség a fordulatidővel és a fordulatszámmal
fejezzük ki. Egy teljes kör megtétele a fordulat (revolution). Egy fordulat
megtételéhez szükséges idő a fordulatidő (periódusidő); jele: T. Az
időegység alatti fordulatok száma a fordulatszám; jele: f; szokásosan a
percenkénti fordulatszámot adjuk meg.
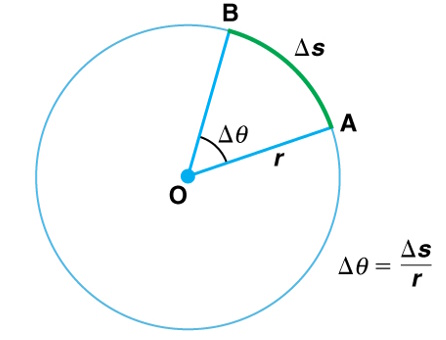 forgásszög rotational angle az elfordulás nagysága, amely megfelel a forgó test
által megtett szögfordulásnak. Jele: Δθ; egyenlő Δs
/ r (a Δs az ívhossz [a forgó test által megtett körívnek a hossza], az r
a kör sugara [radius]). (Az ábrát Teleki Katalin készítette.) (→kör)
forgásszög rotational angle az elfordulás nagysága, amely megfelel a forgó test
által megtett szögfordulásnak. Jele: Δθ; egyenlő Δs
/ r (a Δs az ívhossz [a forgó test által megtett körívnek a hossza], az r
a kör sugara [radius]). (Az ábrát Teleki Katalin készítette.) (→kör)
szöggyorsulás angular acceleration a szögsebesség időbeli változásának a gyorsasága. Jele: β, mértéke: Dω / Dt (a Dω a szögsebesség megváltozása, a Dt a megváltozás időtartama. Mértékegysége: 1/s2.
szögsebesség angular/rotational velocity a szögelfordulás időbeli változási sebessége. Jele: ω; mértéke: Δθ / Δt (a Δθ a forgásszög változása, a Dt a változás időtartama). Mértékegysége: 1/s.
forgástengely (tengely) a forgó testnek a mozdulatlanul maradó vonala; a test ekörül forog.
gyulladásállapot* low grade systemic inflammation a szervezet olyan állapota, amelyben a gyulladáskor keletkező molekulák (IL6, IL1β, IL18, CRP- [high-sensitivity C-reactive protein] TNFα stb.) és sejtek (fehérvérsejtek, egymagúak, nagyfalósejtek stb.) felszaporodnak, de a gyulladásra jellemző panaszok, tünetek és szövetelváltozások (fájdalom, duzzadás, pír, láz) nem alakulnak ki; ezért nem nevezzük gyulladásnak. A keringéssel szállított gyulladásmolekulák befolyásolják más sejtek működését, és előbb-utóbb kóros elváltozásokhoz, betegséghez vezetnek (→szív- és érbetegségek). Jellemzi a gyulladásállapotot a szabadgyökök képződése és az immunfelügyelet csökkenése is; mindkettő elősegíti a rákképződést. Gyulladásállapotot okoz a zsírtöbblet, a rosszindulatú daganatok, a szövetelhalások, az idült fertőzöttség, az állandósult allergia, de ide sorolják az öregséget is.
A gyulladásállapot klinikailag nem vehető észre; szokásosan laboratóriumi vizsgálatokkal, a szérumban lévő gyulladásjelzőkkel kórismézzük. Ezek közül a CRP a legjelentősebb, amelyet az FVS (fehérvérsejtszám) jól kiegészít. Közéjük tartoznak még az IL6 és a TNFα, és a szabaddá vált adhéziós molekulák (VCAM1, ICAM1, E-szelektin) mérése is. Jellemző a gyulladásállapotra még a csökkent HDL-koleszterin-szint.
Hassall-testek Hassall’s corpuscles (→csecsemőmirigy)
Hoogsteen-féle hidrogénkötések Hoogsteen hydrogen bonds a DNS-ben előforduló olyan hidrogénhidak, amelyek mások, mint a DNS szálait összekötő, vagyis az adenin és a timin, illetve a guanin és a citozin között létrejövő hidrogénkötések (Watson–Crick-féle hidrogénkötések). Ilyenek alakulhatnak ki, pl. ha a purinbázis elfordul, és az 5-ös gyűrűje kapcsolódik pirimidinhez, nem pedig a hatos gyűrű, avagy két azonos purinbázis (adenin–adenin; guanin–guanin) között stb. (→G-négyes)
A Hoogsteen-féle hidrogénkötések másodlagos DNS-szerkezeteket hoznak létre a DNS számos helyén. Ezek többnyire ingatag szerkezetek, sokszor csak átmenetiek, de a hozzájuk kapcsolódó fehérjék rögzíthetik, állandósíthatják.
Jelentősen megváltoztathatják a bázispár viszonyait is, ami befolyásolhatja a fehérjék általi felismerésüket, a DNS-hibajavítást, a DNS-kettőződést. (→DNS-szerkezet)
hysteroplasty →méhhelyreállító műtét
kettőződési
testecs* replisome (repliszóma)
a DNS kettőződését irányító sajátos fehérjék összeállása. Minden sejtben van, a
sejt megfelelő osztódásának a kulcsa. Törzselemei emberben: a DNS-polimeráz,
helikáz, primáz, kettőződési gyűrű (circular
sliding clamp), a kettőződési gyűrűirányító (clamp loader) és SSB fehérjék (single-strand
DNA binding protein).
▪ DNS-polimeráz. A sejtekben sokféle DNS-polimeráz van, a magsejtű DNS megkettőződésében a DNS-polimeráz-α és -δ hozza létre az új DNS-szálakat. Szükséges hozzá ATP, magnéziumion és az eredeti DNS szál (mintaszál).
A polimeráz nukleotidot köt a nukleotidsor 3’-végén lévő szabad hidroxil (OH) csoportjához. Minthogy a DNS-polimerázok két szabad nukleotidot nem képesek összekötni, csak már meglévő nukleotid lánchoz kapcsolnak újabb nukleotidot, az új DNS-szálat önmagában nem hozhatják létre: szükségük van egy indító bázissorra (primer), amely egy 10-12 nukleotid hosszú RNS-szakasz. Az indító RNS-szakasz nukleotid sorrendje a mintául szolgáló DNS-szál kiegészítője, és szabad 3’-OH csoporttal végződik. Az új DNS-szál minden nukleotidja úgy kötődik, hogy azok kiegészítő bázisai szembe kerülnek az eredeti – a minta – DNS-szál bázisaival, a kapcsolatokat pedig hidrogénhidak rögzítik. A következő nukleotid csak a hidrogénhidak kialakulását követően kapcsolódhat.
▪ DNS-helikáz fehérjeössztes, az MCM2–7 hatosból, a CDC45-ből és a GINS-fehérje csoportból (SLD5, PSF1–3) épül fel – együtt CNG-össztes a nevük. A DNS-hez a kettőződési előzetes kialakulásával kötődik, az G1 szakaszban. A kettőződési testecs törzseleme.
▪ RNS-primáz. A DNS-képződés megkezdéséhez szükséges kis – 12 nukleotidból álló – RNS-indítót (primer) hozza létre.
▪ A kettőződési gyűrű* (circular sliding clamp) gyűrű alakú fehérje, amely körbefogja a DNS-t és rögzíti a DNS-polimerázt a DNS-hez..
▪ A kettőződési gyűrű irányítójaFZs (clamp loader) a kettőződési gyűrűt nyitja, zárja a DNS körül ATP felhasználásával.
▪ Az SSB fehérjék a szétalakult, DNS egyszálú jellegét őrzik meg és megelőzik a kiegészítő egyszálú DNS molekulák újrakapcsolódását.).
A kettőződési testecs tevékenységében a törzsfehérjéken kívül sok egyéb fehérje is közreműködik, meglehetősen változékony módon.
Ha két kezdőponttól történő másolódás találkozik, a kettőződési villák összeérnek, befejeződik a kettőződés; a kettőződésössztest el kell távolítani. Ennek folyamata kevéssé ismert. A helikáz eltávolításának feltétlen szerepe van, ismert az MCM7 sokszoros ubikvitines bontása.
kiterjedéstelen mennyiség dimensionless quantity (→kiterjedés, mennyiség)
magtestetcs nucleosome a hisztonmagból és a köré tekeredett DNS-ből álló képződmény. (→kromatinszerkezet)
másulásteher (daganat-másulásteher) tumor mutational burden, TMB a daganatsejtekben előforduló DNS-másulások teljes száma. Gyakorlati jelentősége van: lehet daganatjelző, de fontos a kezelés szempontjából is, pl. azok a ráksejtek, amelyekben sok másulás van (túlmásulás, halmozott másulás) általában érzékenyek immunkezelésre.
Mayer–Rokitansky–Küster–Hauser-kór (MRKH-kór) a Müller-cső ritka (1/5000 nő) fejlődési rendellenessége. A hüvely felső harmadának hiánya és a méh hiánya vagy csökevényes volta jellemzi. A csonkméh sem működik, a betegeknek nincs vérzésük; szokásosan az elsődleges vérzéshiány miatti vizsgálatok derítenek rá fényt. Nagyritkán előfordul, hogy a csökevényes méhben keletkezik nyálkahártyaféleség, és az a havibajnak megfelelően le is válik, de kiürülni nem tud, görcsöket okozhat. A vér általában felszívódik, a nyálkahártyaszigetek pedig előbb-utóbb elpusztulnak. Egészen kivételes, hogy vérömleny keletkezik.
A külső nemi szervek és a hüvely alsó harmada ép, miként a petefészkek is, ezért a másodlagos nemi szervek is szabályosan kifejlődnek.
A felső vizeletrendszer hibái 30%-ban fordulnak elő, a vesehiány vagy a vese felszállásának elmaradása miatt medencei vese (ectopic pelvic kidney) a leggyakoribb. Kromoszóma-rendellenesség nincs. 46 XX a kromoszómaszerkezet.
Két, az I-es és a II-es formáját különböztetik meg: a II-es az I-estől annyiban tér el, hogy egyéb rendellenességek is társulnak hozzá. Ezek sokfélék lehetnek: vese-, csontrendszeri és szívfejlődési zavarok. Gyakori még a halláscsökkenés. Az I-es formájú MRKH-kór a gyakoribb.
Különleges formája a II-es MRKH-kórnak a MURCS (Müllerian duct agenesis, renal agenesis, cervicothoracic somite dysplasia); igen súlyos veleszületett rendellenességek jellemzik.
méhhelyreállító műtét metroplasty, uteroplasty, hysteroplasty a méh veleszületett rendellenességeinek helyreállító műtéteit foglalja magában.
molekulabeli térhelyzet stereochemistry (sztereokémia)
az atomok térbeli elrendeződését vizsgálja egy molekulán belül. Három formája
van:
▪ Téralap (constitution,
konstitúció) az atomok kapcsolódási sorrendje egy molekulán belül.
▪ Téralkat (conformation, konformáció) az
egymással közvetlen kapcsolatban nem lévő atomok egymáshoz való elhelyezkedése.
Ez is befolyásolja a molekulák tulajdonságát. A nyújtott, nyitott téralkat
rögzültebb szerkezet, mint a zárt, ahol az egyes molekularészek egymáshoz
közelebb vannak.
▪ Térközponti helyzet (configuration, konfiguráció).
Akkor alakul ki, amikor egy adott szénatomhoz négy különböző csoport
kapcsolódik. Az ilyen szénatomot központi szénatomnak nevezzük.
A molekulák térhelyzetének a szerepe meghatározó a molekulák működésében, kapcsolódásában más molekulákkal, például a fehérjék működését térhelyzeti változások irányítjuk. A nem megfelelő térhelyzetű fehérje működésképtelen. Jelentős továbbá a molekulák felismerése szempontjából is, például az enzimek ugyanannak a vegyletnek csak az egyik térszerkezetű változatát azonosítják.
nested gene beágyazódott génSP (→gén)
nukleoszóma nucleosome →magtestecs
nyirokrendszer lymph/lymphatic system a nyiroksejteknek a szöveteket behálózó, különleges anatómiai rendszere. Feladata a kórokozók, az idegen vagy a kóros saját sejtek és molekulák felismerése és elpusztítása. Részei: a nyirokszervek, a nyálkahártyai (MALT) és a bőrhöz társult nyirokszövet (SALT), a szervezetben szétszóródott (őrjáratozó) nyiroksejtek, valamint a nyirok- és a vérkeringés.
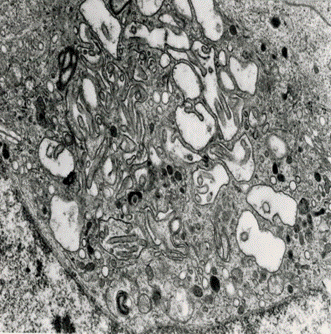 peroxitestecs* peroxisome (
peroxitestecs* peroxisome (peroxisoma, peroxiszoma)
0,2–1 μm nagyságú, egyetlen hártyával határolt, közepesen sűrű, finoman
szemcsés fehérjedús állományú, számváltoztató szervecske. A magvas sejtekben
általánosan előfordul. Számuk sejtfajtákként, de a körülményektől függően, a
szükségletek szerint is változik. Egy-egy sejtben 100-tól 1000-nél is több
lehet; a legtöbb a májsejtekben és a vesecsatornák sejtjeiben van. Az
elektronmikroszkópos felvételen csecsemőmirigy hámsejtje látható. A sima
felszínű plazmahálózat között a gömb és tojás alakú fekete pöttyök a
peroxitestecsek. (Oláh Imre felvétele.)
A peroxitestecsek állományát (matrix) fehérjék alkotják. Legalább 50-féle enzim van bennük; többek között peroxidázok (nevét innen kapta) és kataláz. A peroxidázok hidrogént vonnak el oxigén hozzáadásával, a keletkezett káros hidrogénperoxidot (H2O2) pedig a kataláz bontja vízre és oxigénre, vagy használnak más molekuláktól való elektronelvonásra. Tartalmaznak egyéb oxidázokat (zsírsav-oxidáz, urát-oxidáz, D-aminosav-oxidáz stb.) is. Az enzimek részben fajlagosak, mások más szervecskében, pl. az energiatermecsben is előfordulnak.
Ezek az enzimek a vegyületek sokaságát bontják (pl. aminosavakat, zsírsavakat), számos anyagcsere-folyamatban, köztük az energia, a szabadgyökök és a lipidek anyagcseréjében meghatározok; pl. a zsírsavak β-elektronleadási folyamatait irányítják; a szabadgyökök képződését gátolják vagy serkentik szigorú szabályozással. Részt vesznek továbbá a plazmalogen (az idegek mielin-/velőshüvelyének alapanyaga), az epesavak, koleszterin, gyulladásmolekulák (pl. leukotrin) és az idegműködést szabályozó dokozahexaénsav (DHA) képzésében. Fontos szerepük van a gyulladásos és vírusellenes folyamatok jelközvetítésében. A peroxitestecsek tehát a sejtanyagcsere központi szervecskéi; sokoldalú feladatukat az energiatermecsekkel, a plazmahálózattal, a lipidcseppekkel és a bontótestecsekkel együttműködésben látják el.
A peroxitestecs külső ingerek hatására képes növekedésre és többszöröződésre; az ingerhatás multával pedig lebontásra kerül (pexophagy) – ezért mondjuk számváltoztatónak. Többszöröződéskor a hártya megnyúlik, majd egy ponton összeszűkül és lefűződik, de keletkezhetnek újonnan is a plazmahálózatból. Kialakulásukban, szétválásukban és tevékenységükben sajátos fehérjék működnek közre, amelyeket peroxinoknak (peroxisomal/peroxisome biogenesis factors) nevezünk. Ezek szállítják a fehérjéket a peroxitestecs állományába és hártyájába is. (→peroxinok)
A peroxitestecs elégtelen működése súlyos anyagcserezavart és fejlődési hibákat okoz; ha ezt a peroxinok másulása vagy hiánya okozza, peroxitestecs-képződési kórképről van szó (peroxisome biogenesis disorders, PBDs). Ilyenek a Zellweger-kórképek, az RCDP, magyarul rövidvégtagos porcosodászavar, a Heimler-kór és valószínűleg mások is. (→Zellweger-kórképek, RCDP, Heimler-kór). Peroxitestecs működési zavart a kataláz elégtelensége is létrehozhat.
peroxiszóma →peroxitestecs
pro- előtag;
’előforma, megelőző’ jelentésű ■ progenitor →előalak ■ prognosis →kórjóslat ■ progression →előrehaladás ■ progression-free survival (→túlélés) ■ prokaryocyte,
prokaryote (prokariocita, prokariota) →maghíjas
■ prokollagén (→kollagén)
■ proliferation →burjánzás ■ promoter →indító
■ prophylaxis →megelőzés ■ prospective (→előretekintő)
■ prosthetic group tartozékcsoport (→enzimszerkezet) ■ proteomer néhányas fehérje ■ proteosome →fehérjetestecs (proteoszóma) ■ proteosome-shuttling factor (→fehérjetestecs-szállító jelfogó) ■ proteolysis →fehérjebontás ■ proteome (proteom) →képzett összfehérje ■ proteomer →fehérjenéhányas ■ proteomics képzett összfehérjék tanulmányozása ■
protooncogene daganatossággén ■ protozoon →egysejtű
rendezetlenség state of disorder of a system/substance hőtani fogalom: az anyag/rendszer atom/molekula szintű szerkezete. Ha az atomok és/vagy molekulák közel állnak egymáshoz, erősen kötődnek, tehát rögzültek, a rendszer szerkezete rendezett, bonyolultnak mondjuk. Ha az atomok/molekulák szabadon mozognak, egymáshoz lazán kapcsolódnak, a rendszer szerkezete rendezetlen; egyszerűnek mondjuk. A legbonyolultabb a kristályok szerkezete: atomjaik/molekuláik erős kötésekkel szorosan kötődve szabályos szerkezetet alakítanak ki. Például a gyémánt, amely kis atomok szoros kötelékéből áll. A szilárd testek kevésbé rendezettek, még kevésbé a folyadékok. A gázok szerkezete rendezetlen, benne az atomok, molekulák fékezetlenül mozognak. A rendezetlen szerkezet térfogata nagyobb, mint az ugyanolyan összetételű rendezetté.
A rendezetlen szerkezet energiaigénye jóval kisebb, mint a rendezetté, ezért a rendszerek a rendezetlenség irányába változnak: a kevés energiát igénylő egyensúlyállapot kialakítására törekszenek.
rendszer, környezet system, surroundings természettudományi fogalmak. A rendszer a világ (az anyagi valóság) vélt vagy valós határfelülettel elkülönített része, amelyet magunk választunk ki. Ilyen értelemben számtalan rendszer lehet, fizikai, vegyi és biológiai rendszerek sokasága. Például kémcsőben lévő folyadék, terem és tartozékai, vagy akár a Föld légköre, avagy gáz a léggömbben rendszer (a gáz eloszlásának, mozgásának és a léggömb falának a rendszere). Ami a rendszeren kívül van, az a környezet (surroundings). Vegyi rendszer például a vegyi anyagok keveréke, környezete az edényzet és minden más körülötte. Biológiai rendszer például a nyirokkeringés, az immunsejtek rendszere, környezete a szervezet többi része. Elemi biológiai rendszer a sejt; környezete a sejtkörüli állomány.
A rendszert állapotjellemzőkkel írjuk le, mint
hőmérséklet (T), nyomás (p), térfogat (V), anyagmennyiség (n) stb. Ennek
alapján lehet állandó nyomású (izobar), állandó hőmérsékletű (izoterm)
és állandó térfogatú (izochor).
A rendszer és a környezet kölcsönhatása szerint háromféle rendszert különböztetünk meg: elszigetelt, zárt és nyílt rendszert.
▪ Elszigetelt a rendszer, ha a határfelületén sem anyag, sem energia nem léphet át. Tehát a rendszerrel energiát sem közölhetünk, és nem is vonhatunk el.
▪ A zárt rendszer határfelületén energia átléphet, de anyag nem. Tehát energiát cserélhet a környezetével, például melegítjük. A zárt rendszer lehet állandó és változó térfogatú. Állandó például egy lezárt kémcső; térfogata nem változik. A dugattyús henger térfogata változik, függően a dugattyú állásától.
▪ A nyílt rendszer határfelületén az anyag is átléphet, nem csak az energia. Ilyen például egy folyadékot tartalmazó nyitott kémcső. Adhatunk hozzá vagy kiönthetünk belőle folyadékot. Melegítéssel pedig energiaváltozást idézünk elő.
A biológiai rendszerek nyílt rendszerek.
A
kölcsönhatást a rendszer fala határozza meg, például a hő szempontjából a fal
lehet hőszigetelő (adiabatikus) – ilyen az elszigetelt rendszer fala;
féligáteresztő (szemipermeábilis) vagy éppen hővezető.
A rendszereket csoportosíthatjuk a rendszer mérhető tulajdonságainak térbeli eloszlása szerint is:
▪ Egynemű rendszer homogeneous system (homogén
rendszer): mérhető tulajdonságai (állapotjellemzői) minden ponton
egyformák. Például egy jól elegyített oldat – hőmérséklete, nyomása stb. minden
részében azonos.
▪ Egyenetlen rendszer nonhomogeneous system (inhomogén
rendszer): mérhető tulajdonságai folyamatoson, lépésről lépésre változnak.
Például ha egy fémdarabot melegítünk, annak hőmérséklete folyamatosan nő, nem
ugrásszerűen változik.
▪ Egyveleg rendszer heterogeneous system (heterogén
rendszer): mérhető tulajdonságai ugrásszerűen változnak. Például olvadó
jég, amely az olvadása egy pontján folyadékká (víz) alakul, állapota
ugrásszerűen változik. Egyveleg, mert szilárd és folyékony összetevői is
vannak.
rendszerállapot* system state, thermodinamic state a rendszer mérhető fizikai tulajdonságainak összessége egy adott pillanatban. Függetlenül attól, hogy az állapot miként alakult ki.
rendszeregyensúly* system equilibrium a rendszert alkotó részecskék egyenletes eloszlása. Az állapothatározók egyike sem változik.
ribosome (riboszóma)
→ribotestecs
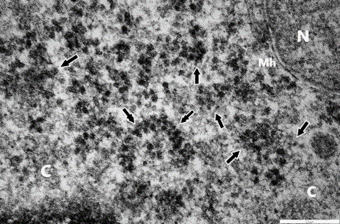 ribotestecs ribosome (
ribotestecs ribosome (riboszóma) csak elektronmikroszkóppal látható
(~25 nm), zömében rRNS-ekből, kisebb részben fehérjékből felépülő,
önszerveződő, nagy enzimössztes (2–3 millió Da); alkotóelemeiből magától
összetevődik. Két különböző méretű alegységből áll. Az elektronmikroszkópos
felvételen a ribotestecsek egy részét nyilak jelölik. A kettős nyíl jelzi azt,
amelyben az mRNS a metszet síkjában fekszik. A ribotestecs a két alegység
határán kötődik az mRNS-hez. A mRNS domború oldalán helyezkedik el a nagyobbik,
míg a kisebbik alegység a homorú oldalon van. Valószínűleg, a két alegység
méretbeli különbsége idézi elő a mRNS hajlását.
N = sejtmag; Mh = maghártya; C = sejtplazma. (A felvételt Oláh Imre készítette.)
Az alegységeket ülepedési együtthatójuk (Svedberg-egység, S) szerint különböztetik meg. Az emberi ribotestecs 80S (a nagyobb alegysége 60S, a kisebb 40S) nagyságú. A nagyobb három rRNS-ből (5S, 26S és 5,8S) és 50 fehérjéből; a kisebb egy rRNS-ből (18S) és 35 fehérjéből tevődik össze. A ribotestecs két alegysége a sejtplazmában külön áll; az átfordítás folyamatában egyesül az mRNS-hez kapcsolódva.
A sejtekben több millió ribotestecs van, a sejtállomány egynegyedét is kitehetik. A sejtmagvacskában tevődnek össze, a maghártya járatain jutnak a sejtplazmába. Zömében a plazmahálózat) hártyájához kötődnek (durva felszínű plazmahálózat), de a sejtplazmában szabadon is előfordulnak, és az energiatermecsben is megtalálhatók.
A ribotestecs a fehérjeképzés, az mRNS átfordításának, a polipeptid kialakításának a helye: lényegében az aminosavakat peptidkötéssel kapcsoló óriás enzim; ribozim. A kis alegység az mRNS-t és az aminoacil-tRNS-t kapcsolja, a nagy alegység a peptidkötéseket hozza létre. Az aminoacil-tRNS olvassa le a ribotestecshez kötődött mRNS kódját, és rakja az aminosavakat ennek megfelelően egymás mellé.
A ribotestecsben a tRNS kapcsolódására három hely van (A, P, E): az A-hely az aminoacil-tRNS kötődési helye, a P-helyhez a peptidil-tRNS, az E-helyhez pedig az elváló (exit) tRNS kötődik. (→átfordítás)
A fehérjék 99%-a a sejtplazmai, főleg a plazmahálozathoz kötődött ribotetecsekben keletkezik. Az energiatermecsekben lévő ribotestecsekben kevesebb mint tízféle fehérje képződik (energiatermecsi fehérjék*); ezek az fehérjeállomány <1%-át teszik ki.
rRNS (ribotestecs-ribonukleinsav) ribosomal RNA, rRNA nem kódoló RNS, a ribotestecs alkotója. Ribozim, azaz enzimhatású, pl. észterkötéssel kapcsol össze aminosavakat. A ribotestecset alkotva tevékenykedik (→ribotestecs).
Az elsődleges szerkezetében szárhurkok keletkeznek bázispárosodással, hasonlóan a miRNSekhez; ezek teszik lehetővé a térszerkezet kialakulását, a fehérjék szoros kapcsolódását.
Az rRNS gének kódolják, amelyek fej–láb kapcsolódásban vannak a magvacskában, és a velük társuló fehérjékkel, valamint az általuk kódolt rRNS-ekkel együtt alkotják a magvacskát. A különféle sejtekben nem mindegyik rRNS gén tevékeny. A gént az RNS-polimeráz-1 írja át elsődleges rRNS-re (47S rRNS-átirat – az S az ülepítés Swedberg-egysége). Az átalakuló 47S rRNS-átiratból RNS-kivágással 28S, 18S és 5,8S rRNS keletkezik, amelyeket a kis ribonukleoptoteinek (small nucleolar ribonucleoproteins, snoRNPs) és egyéb alakítófehérjék (protein processing factor) formálnak 60S (~3000 nukleotid) és a 40S (~1800 nukleotid) nagyságúvá, a ribotestecs két alegységének megfelelően. A magvacskában a 60S és a 40S rRNS-ekhez szállítófehérjék kötődnek; így jutnak a sejtplazmába a ribotestecs kialakítására. Az rRNS a sejt RNS-einek 80%-át adja, mintegy 10 millió van egy sejtben.
RSK (ribotestecsi S6-kináz, p90S6K) ribosomal (rp) S6 kinase, rpS6 90 kDa nagyságú törzsökös szerin-treonin-kináz. N-végi sarkalló gomolya (catalytic N-terminal kinase domain, NTKD) és C-végi, tevősítő gomolya (activating C-terminal kinase domain, CTKD) van, amelyeket összekötő rész kapcsol egybe. Négyféle, RSK1–4 hasonmás ismert, enzimcsaládot alkotnak. Noha a négyféle RSK szerkezete nagyon (~80%) hasonló, tevékenységük különböző: sejtfolyamatok szerint fajlagos. Az RSK1–2 daganatserkentő, az RSK 3–4 daganatgátló hatású.
Az RSK1–3 a MAPK-jelközvetítésben vesz rész: a MAPK a C-végi gomolyhoz kapcsolódik, és foszforilezi a gomoly és az összekötő rész szerin-treonin aminosavait. Ennek következtében PDK1 kötődik az RSK-val, és foszforilezi a sarkalló gomolyt. Így válik teljesen tevékennyé. A serkentett RSK számos, az átírásban, átfordításban, a sejtkör szabályozásában és a sejttúlélésben résztvevő fehérjét szabályoz foszforilezéssel. Az RSK4 elsődlegesen a magzatfejlődésben vesz részt. (→MAPK, PDK1, ribotestecs)
SI (Système international d’unités, International System of Units) →mértékegységrendszer
síkvonalas rendszer* a Descartes-féle coordinate systems egyike: két egymásra merőleges számegyenes; metszéspontjukat (O pont) kiindulási pontnak (point of origin, origin) nevezzük. A vízszintes tengely az x tengely, a függőleges tengely az y tengely. A tengelyekre pontokat veszünk fel, ezeket nevezzük síkadatoknak* (coordinates).
A rendszerben minden pontot rendezett számpárral (természetes számokkal) adunk meg. A számpár első tagja (első jelzőszám) az x tengelyhez viszonyít, azt mutatja, hogy a vizsgálandó pont, például időpont, milyen messze van az x tengelyen a kiindulási ponttól. A második jelzőszám a y tengelyhez viszonyít: azt jelöli, hogy a pont hány egységnyire van az y tengelyen a kiindulási ponttól. Ha a számpár pozitív, az x tengellyel párhuzamosan jobbra, az y tengellyel párhuzamosan felfelé lépünk. Ha a szám negatív, ellenkező irányban.
A rendszerrel a sík minden pontján megadhatjuk a mennyiségeket (síkmennyiség). Két síkadat, az x és az y tengelyi; a síkbeli mennyiségeket ezekre a síkadatokra állított merőlegesek metszéspontjai adják meg. Másként: a síkvonalas rendszerben két számhoz rendelünk egyet. Mivel egész számokkal számolunk, a rendszert egész számokkal jelöljük, például (3, 5), a metszésvonal síkadatai. A 3 az x tengely síkadata (mondjuk időpont), az 5 az y tengely síkadata (mondjuk gyógyszermennyiség). A metszésvonaluk 3 és 5. Ennek megfelelő a 3 időegységben lévő gyógyszermennyiség. A kezdőpont síkadata természetesen 0.
térazonmások*
stereoisomers (sztereoizomerek) azonos összetételű, azonos kötéssorrendű, de eltérő
térelrendeződésű vegyületek. A térszerkezeti különbség lehet az
elektronkötésben lévő és a nem elektronkötésbén lévő atomok és/vagy molekulák
között. Az előbbieket téralakzati azonmásoknak, az utóbbiakat térhelyzeti
azonmásoknak nevezzük. (→téralakzati azonmások, térhelyzeti azonmások)
térhatás allostery a több kötőhelyes fehérje (nagymolekula) egyik kötőhelyéhez kapcsolódó molekula hatásának áttevődése a fehérje másik kötőhelyére. Úgy jön létre, hogy a több kötőhelyes fehérjének egyik kötőhelyéhez kapcsolódó molekula kivált olyan térhelyzeti átalakulást, amely befolyásolja a fehérje másik kötőhelyével kapcsolatos tevékenységét. Szokásosan a szabályozóhelyhez (allosteric site) kapcsolódó molekula hat a hatáshelyre, lehetővé téve a fehérjeműködés szabályozását (térhelyzeti szabályozás).
térhelyzeti szabályozás* allosteric regulation az enzimnek vagy más ily módon szabályozható fehérjének a szabályozóhelyhez kapcsolódó molekula által előidézett térhelyzeti változása, amely serkentheti vagy gátolhatja az adott fehérje működését. A fokozást kiváltó molekula a térhelyzeti serkentő* (allosteric activator), a gátlást okozó a térhelyzeti gátló* (allosteric inhibitor) molekula.
A szabályozóhelyhez kapcsolódó molekula csak egy irányban hat: vagy serkent, vagy gátol. Enzimek esetében a serkentés általában a vegylet kapcsolódását mozdítja elő, pl. bizonyos enzimek hatáshelyét lefedi az enzim egyik szerkezeti eleme, de amikor szabályozóhelyhez kötődik molekula, a térszerkezet úgy változik, hogy a hatáshely szabaddá válik, és kötődhet hozzá a vegylet. Előfordul az is, hogy hatóegység tevékenysége fokozódik (Vmax-érték emelése). A gátlás szokásosan a hatáshely változásában nyilvánul meg (fedődhet, változhat a térbeli illeszkedése), ezért az enzim nem képes megkötni a vegyletet.
Az enzimek térhelyzeti szabályozása lehet:
• Visszaható gátlás* (feedback inhibition), amely egy (vagy több együttműködő) enzim hatására képződött termék és az enzim közötti kölcsönhatás eredménye. Ha a termék mennyisége meghaladja a sejt szükségletét, a fölös termék a szabályozóhelyhez kapcsolódva leállítja az enzim működését.
Jellegzetes a visszajelzési szabályozás a többenzimes folyamatoknál: a folyamat végterméke vagy valamelyik köztiterméke az első enzimhez kötődve fékezi az enzimsort.
• A vegyletes térhelyzeti szabályozás* (homotropic allosteric regulation) a vegylet és az enzim közötti szabályozás: a vegylet egyúttal szabályozhat is úgy, hogy a szabályozóhelyhez is kötődhet.
• Másmolekulás térhelyzeti szabályozás* (heterotropic allosteric regulation) a szabályozóhely és olyan molekula kölcsönhatása, amely nem a termék, de nem is a vegylet. Ezt a szabályozómolekulát ezért nevezzük másmolekulának.
▪ Látszólag vetélkedő gátlás*, amely azt jelenti, hogy az egyik kötőhelyhez kapcsolódó molekula kizárja a másik kötőhelyhez való kapcsolódás lehetőségét. Ennek következtében, ha az enzim szabályozóhelyéhez kapcsolódik molekula, az enzim nem képes megkötni a vegyletet, elmarad az enzimhatás; vagy fordítva: a vegylet kapcsolódása akadályozza a másikét. Azért nevezzük a vetélkedést látszólagosnak, mert a molekulák nem ugyanazért a kötőhelyért versengnek.
A fehérjék térhelyzetének megváltoztatása (conformational change) a sejtbiológiai folyamatok egyik leggyakoribb szabályozási formája; a sejtműködés minden formájában meghatározó. Sokszor láncszerűen zajlik, pl. a jelközvetítésben. A jelközvetítés első enzime nem ritkán térhelyzeti szabályozó enzim, amely a serkentő és gátló molekuláinak töménysége alapján érzékeli a környezeti hatásokat, és indítja, gyorsítja, avagy éppen gátolja a jelközvetítést.
A láncfolyamat végterméke is visszahathat az első enzimre: annak szabályozóhelyéhez kapcsolódva gátolja azt (visszaható gátlás); így akadályozza meg, hogy feleslegesen sok végtermék keletkezzék. A láncszerű jelközvetítés gyakorta kétirányú: előfordul, hogy valamelyik molekula, például a végtermék, az egyik irányban gátol, a másikban serkent. Stb.
térszabályozó enzim allosteric enzyme térhelyzeti szabályozással működő, avagy szabályozó térhelyzeti változást kiváltó enzim. Ilyen pl. a G-fehérje-kötő jelfogó, amelynek a térszerkezete megváltozik a jelvivővel kapcsolódva, és ez lehetővé teszi, hogy kötődjék hozzá és tevősödjék a G-fehérje.
szabályozóhely allosteric site a szabályozó molekula kapcsolódásának a helye, máshol van, mint a hatáshely, a fehérjék harmadlagos szerkezete hozza létre. Ha a kötőhelyek más-más polipeptidláncon vannak, a negyedleges térszerkezetnek is szerepe van a szabályozásban. A kötődés a szabályozóhelyekhez ugyanolyan gyenge kötéssel jön létre, mint a vegylet kapcsolásakor, tehát visszafordítható.
térközpont*, térközponti szénatom* stereocenter négy különböző vegységet (atomot és/vagy atomcsoportot) tartalmazó szénatom.
testvérkromatid sister chromatid a kromoszóma két kromatidja egymásnak testvérkromatidja.
tumor mutational burden (TMB) →másulásteher